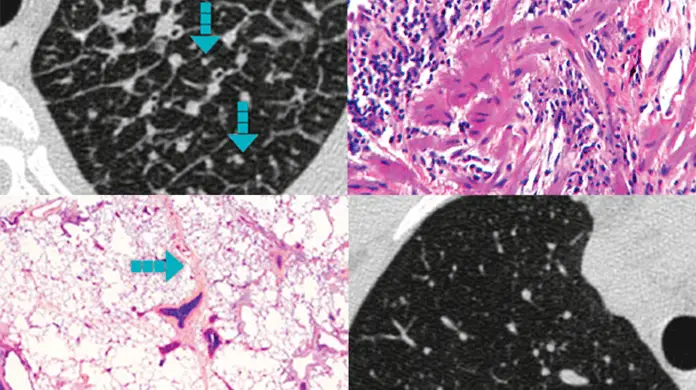
Echipa multidisciplinară
Echipele multidisciplinare pot juca un rol central în diagnosticarea și managementul PID1

DIAGNOSTICUL PID ESTE UN EFORT DE ECHIPĂ2-4

O abordare în echipa multidisciplinară care include un radiolog este cheia pentru diagnosticul precoce și precis al PID cu fenotip fibrozant progresiv5,6

Diagnosticul multidisciplinar este asociat cu niveluri mai ridicate de încredere în diagnostic și reprezintă un acord mai bun între participanți în comparație cu rolurile individuale izolate5,6

Recomandările sprijină o abordare proactivă și colaborativă a diagnosticului precoce și precis al FPI de către o echipă multidisciplinară2,7–11
CARE SPECIALIȘTI AR PUTEA CONSTITUI ECHIPA MULTIDISCIPLINARĂ?
Colaborarea proactivă cu o echipă multidisciplinară de specialiști pentru diagnostic la pacienții cu PID cu fenotip fibrozant progresiv poate reduce riscul de deces al pacientului2,4,6–11
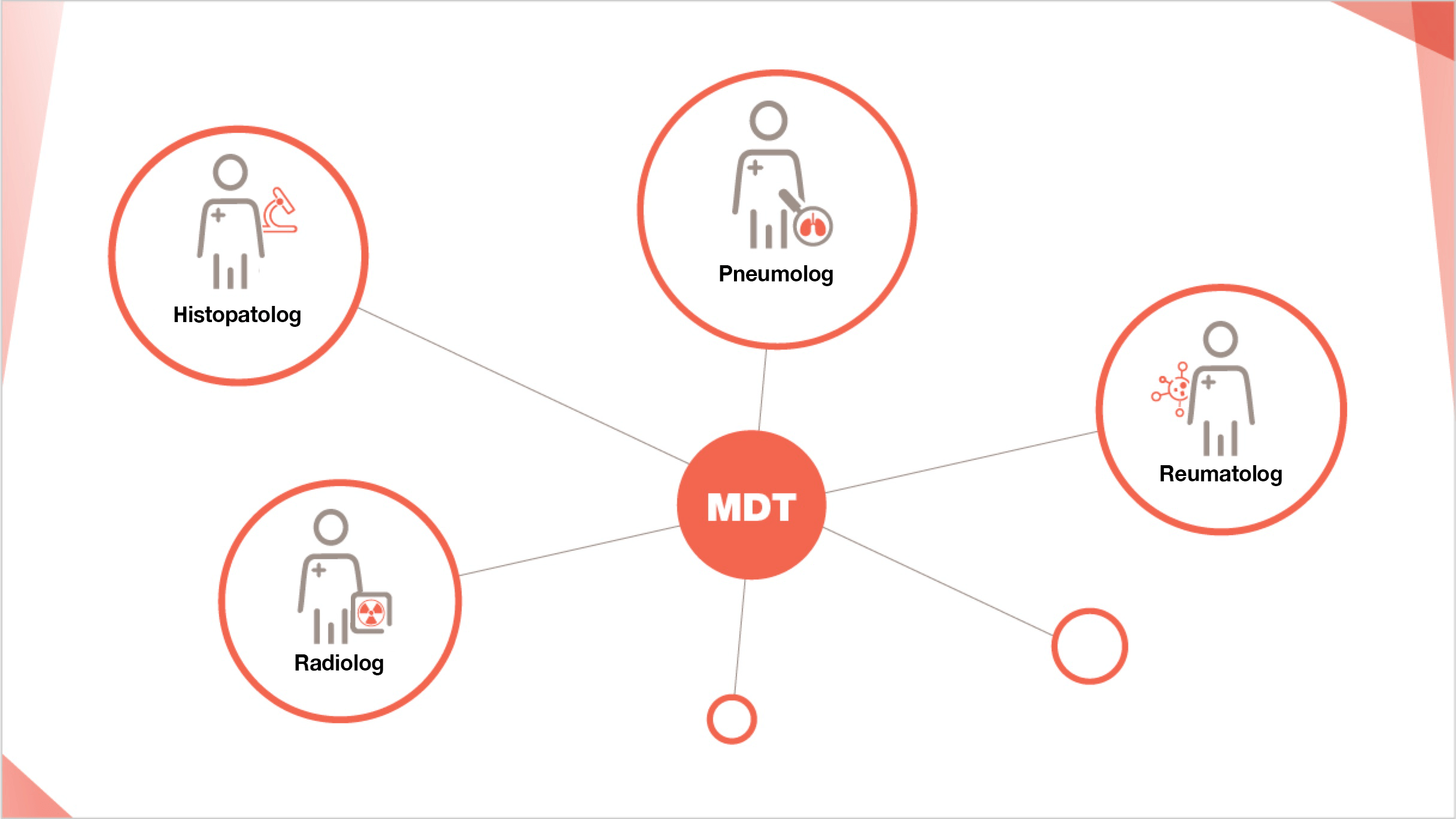
Doar un pneumolog, un radiolog și (în cazurile selectate în care a fost efectuată biopsia) un anatomopatolog ar trebui să fie considerați participanți obligatorii la întâlnirile echipei multidisciplinare.5
CARE INFORMAȚII TREBUIE DISCUTATE DE ECHIPA MULTIDISCIPLINARĂ CÂND SE ANALIZEAZĂ PID CU FENOTIP FIBROZANT PROGRESIV?
Algoritm pentru diagnosticul fibrozei pulmonare1
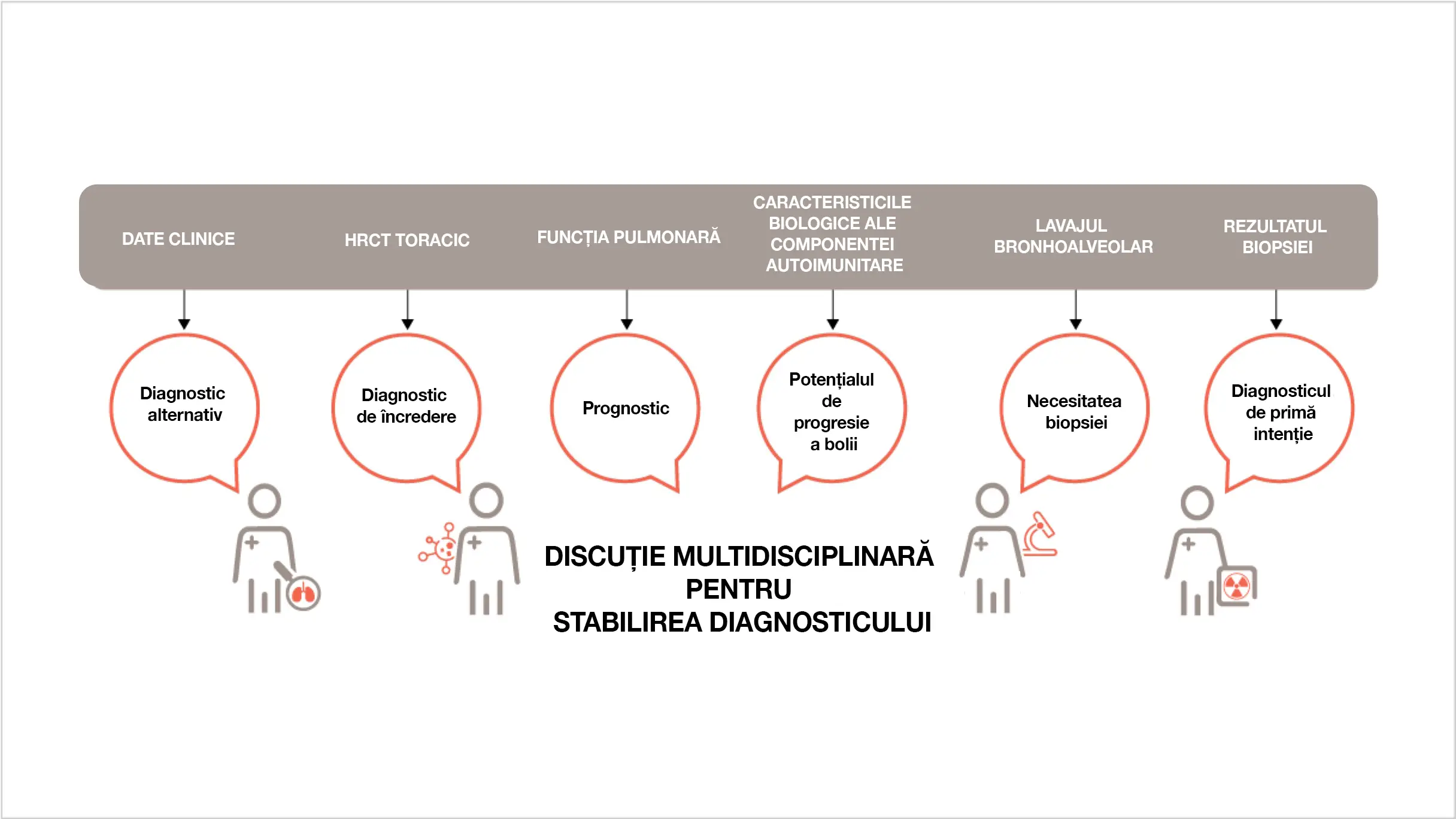
Participanții iau în considerare toate datele disponibile și propun un diagnostic provizoriu de primă alegere, evaluează necesitatea biopsiei și încrederea în diagnostic și iau în considerare posibilele diagnostice alternative.
Dacă un caz nu poate fi abordat de o echipă multidisciplinară, este important ca și clinicianul curant să realizeze că mulți factori trebuie luați în considerare înainte de a putea fi luate decizii de diagnostic.
Adaptat după: Wijsenbeek M, Cottin V. N Engl J Med. 2020;383:958–968.
LA CE ETAPE DE EVALUARE TREBUIE AVUTE DISCUȚIILE MULTIDISCIPLINARE?
Împreună cu evaluarea clinică, modelele de HRCT toracic și discuțiile multidisciplinare facilitează diagnosticul de primă alegere11
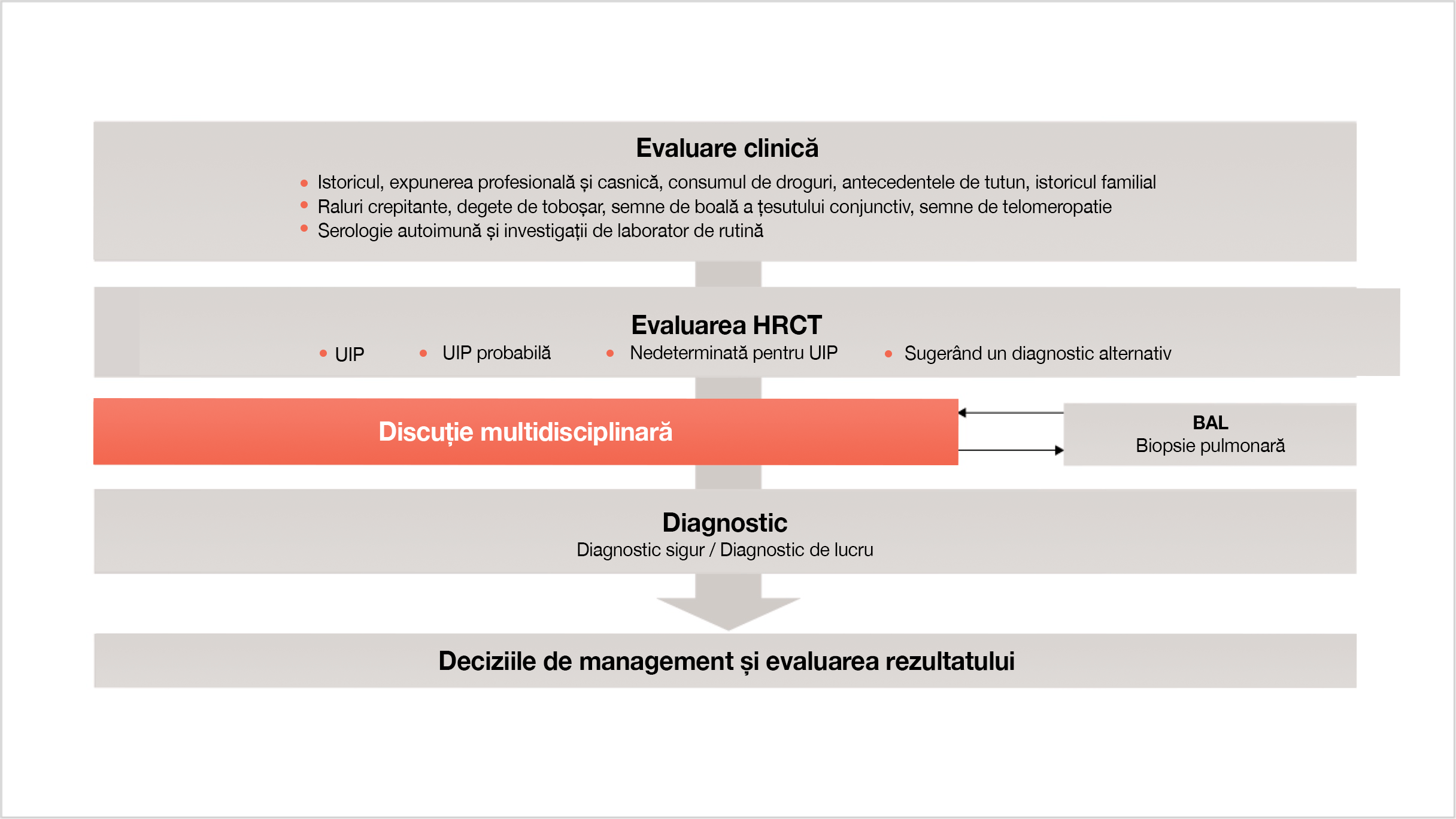
Diagnosticul diferențial optim, precum și gestionarea continuă a PID cu fenotip fibrozant progresiv, pot fi ajutate cu discuții multidisciplinare pe măsură ce noi informații devin disponibile:3,5,11–13
- Discuția în echipa multidisciplinară, care implică contribuțiile expertului radiolog, poate fi necesară pentru a perfecționa în continuare un diagnostic5
- HRCT poate avea un impact semnificativ asupra diagnosticului final, chiar și atunci când un diagnostic histopatologic a fost pus folosind o biopsie pulmonară5
În cazul FPI, întâlnirile echipei multidisciplinare atribuie mai frecvent diagnostice de înaltă încredere, cu semnificație prognostică mai mare, comparativ cu diagnosticele stabilite în aceeași componență dar în mod individual.5
În cazurile în care un MDT este dificil de reunit pentru un pacient cu PID, discuțiile multidisciplinare pot fi conduse virtual sau prin telefon pentru a permite fiecărui specialist să contribuie.12
ÎMBUNĂTĂȚIȚI-VĂ CAPACITATEA DE A DIAGNOSTICA PID CU FENOTIP FIBROZANT PROGRESIV
Aflați mai multe despre HRCT, standardul de aur
CAZURI DE PACIENȚI CU PID PENTRU EVALUARE, DIAGNOSTIC ȘI MONITORIZARE
Descărcați profilurile noastre de pacienți pentru anumite PID specifice pentru a afla despre istoricul medical al pacienților reprezentativi, inclusiv factorii de risc, simptomele prezente, examenul fizic inițial evaluări și constatări diagnostice pe HRCT
Bogdan are FPI
Descărcați cazul clinic al pacientului cu FPI
Carmen are FPI
Cum putem construi o imagine clinică a FPI?
Robert are PHc
Cum putem ajunge la un diagnostic de PHc?
ODATĂ PUS DIAGNOSTICUL, CUM PUTEȚI COMUNICA ACEASTĂ VESTE PACIENȚILOR DVS. CU PID CU FENOTIP FIBROZANT PROGRESIV?
A da o veste proastă este o sarcină de comunicare dificilă și complexă. În seria noastră de filme documentare, profesorul Walter Baile, psihiatru și co-fondator al modelului SPIKES, ne prezintă prin abordarea sa practică cum să structurăm conversațiile dificile.
Modelul SPIKES presupune furnizarea de vești proaste în practica clinică folosind șase elemente: Setare; Percepţie; Invitație/Informații; Cunoştinţe; Empatie; Rezumat/Strategie.14
CUM SĂ TRANSFORMĂM VEȘTILE PROASTE
Capitolul 1 – Provocarea de a comunica vești negative
Profesorul Walter Baile prezintă provocările pe care le implică comunicarea veștilor proaste și ceea ce putem învăța din experiența în oncologie.
Capitolul 2 – Modelul SPIKES în fibroza pulmonară
Comunicarea unui diagnostic cu compasiune poate face diferența. Vedeți de ce profesorul Walter Balle consideră că modelul SPIKES este relevant pentru fibroza pulmonară.
Capitolul 3 – Modelul SPIKES într-un scenariu real
Cuvintele contează. Profesorul Walter Balle descrie o experiență reală despre cum conversația plină de compasiune și sinceră a făcut diferența.
MODELUL SPIKES
Capitolul 1 – Modul SPIKES
O prezentare generală a fiecărui pas al modelului de comunicare SPIKES
Capitolul 2 – SPIKES: Setarea conversației
Configurarea conversației în mod corect pentru a vă ajuta pe dvs. și pacienții dvs. să se simtă relaxați.
Capitolul 3 – SPIKES: Percepția
Cum să determinați ce înțelege pacientul despre situația dată pentru a personaliza conversația.
Capitolul 4 – SPIKES: Invitația
Identificarea modului în care pacientul dvs. ar dori să primească veștile negative
Capitolul 5 – SPIKES: Cunoștințe
Aflați cum să oferiți faptele și informațiile pacientului dvs. într-un mod care funcționează pentru aceștia
Capitolul 6 – SPIKES: Emoții
Descoperiți cum să abordați emoțiile unui pacient cu un răspuns empatic.
Capitolul 7 – SPIKES: Strategie și rezumat
Modul în care elaborarea unui plan pentru viitor vă poate ajuta pacienții să se simtă informați și pregătiți.
Capitolul 8 – Ce vor pacienții de la medicii lor?
Profesorul Balle vă comunică cum să asigurați un parteneriat terapeutic deschis și onest cu pacienții dumneavoastră
Ce alte resurse vă pot ajuta să diagnosticați și să vă gestionați pacienții cu PID fibrozant progresiv?
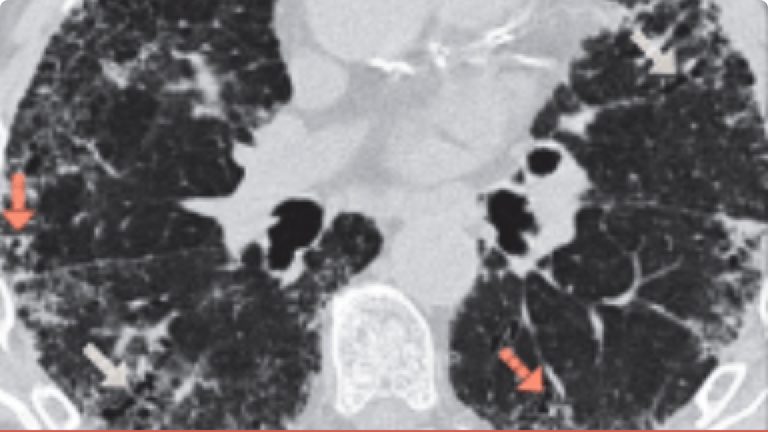
Investigarea PID cu fenotip fibrozant progresiv cu ajutorul imagisticii HRCT
Diagnosticul de PID

IIntervențiile în cazul PID
Note
-
*
Cifre bazate pe un studiu de cohortă prospectiv.
-
BAL, lavaj bronhoalveolar; PHc, pneumonită cronică de hipersensibilitate; HRCT, tomografie computerizată de înaltă rezoluție; PID, pneumopatie interstițială difuză; FPI, fibroză pulmonară idiopatică; MDT, echipă multidisciplinară; UIP, pneumopatie interstițială uzuală.
- Wijsenbeek M, Cottin V. Spectrum of Fibrotic Lung Diseases. N Engl J Med. 2020;383:958–968.
- Raghu G, Remy-Jardin M, Myers JL, et al; on behalf of the ATS/ERS/JRS/ALAT. Diagnosis of Idiopathic Pulmonary Fibrosis. An Official ATS/ERS/JRS/ALAT Clinical Practice Guideline. Am J Respir Crit Care Med. 2018;198(5):e44–e68.
- Cottin V, Hirani N, Hotchkin D, et al. Presentation, diagnosis and clinical course of the spectrum of progressive-fibrosing interstitial lung diseases. Eur Respir Rev.
- Wong AW, Ryerson C, Guler S. Progression of fibrosing interstitial lung disease. Respir Res. 2020:29;21(1):32.
- Walsh SLF. Multidisciplinary evaluation of interstitial lung diseases: current insights. Eur Respir Rev. 2017;26:170002.
- De Sadeleer LJ, Meert C, Yserbyt J, et al. Diagnostic ability of a dynamic multidisciplinary discussion in interstitial lung diseases: A retrospective observational study of 938 cases. Chest. 2018;153(6):1416–1423.
- Raghu G, Collard HR, Egan JJ, et al; on behalf of the ATS/ERS/JRS/ALAT Committee on Idiopathic Pulmonary Fibrosis. An official ATS/ERS/JRS/ALAT statement: idiopathic pulmonary fibrosis: evidence-based guidelines for diagnosis and management. Am J Respir Crit Care Med. 2011;183(6):788–824.
- Martinez FJ, Collard HR, Pardo A, et al. Idiopathic pulmonary fibrosis. Nat Rev. 2017;17:17074.
- Molina-Molina M, Aburto M, Acosta O, et al. Importance of early diagnosis and treatment in idiopathic pulmonary fibrosis. Exp Rev Resp Med. 2018;12(7):537–539.
- Jo HE, Glaspole IN, Levin KC, et al. Clinical impact of the interstitial lung disease multidisciplinary service. Respirology. 2016;21(8):1438–1444.
- Cottin V, Valenzuela C. Diagnostic approach of fibrosing interstitial lung diseases of unknown origin. Presse Med 49. 2020;https://doi.org/10.1016/j.lpm.2020.104021.
- Chung JH, Goldin JG. Interpretation of HRCT Scans in the Diagnosis of IPF: Improving Communication Between Pulmonologists and Radiologists. Lung. 2018;196:561–567.
- De Lorenzis E, Bosello SL, Varone F, et al. Multidisciplinary Evaluation of Interstitial Lung Diseases: New Opportunities Linked to Rheumatologist Involvement. Diagnostics. 2020;10:664;doi:10.3390/diagnostics10090664.
- Kaplan M. SPIKES: a framework for breaking bad news to patients with cancer. Clin J Oncol Nurs. 2010;14:514–516.
- Brauner M, et al. Imagerie des pneumopathies infiltrantes diffuses. Press Med. 2010;39:73–84.
- Flaherty KR, Brown KK, Wells AU, et al. Design of the PF-ILD trial: A double-blind, randomised, placebo-controlled phase III trial of nintedanib in patients with progressive fibrosing interstitial lung disease. BMJ Open Resp Res. 2017;4(1):e000212.
- Theodore AC, Tseng C-H, Li N, Elashoff RM, Tashkin DP. Correlation of cough with disease activity and treatment with cyclophosphamide in scleroderma interstitial lung disease: findings from the Scleroderma Lung Study. Chest. 2012;142(3):614–621.
- Hoffmann-Vold AM, Fretheim H, Halse AK, et al. Tracking impact of interstitial lung disease in systemic sclerosis in a complete nationwide cohort. Am J Respir Crit Care Med. 2019;200:1258–1266.
- Hoffmann-Vold AM, Maher TM, Philpot EE, et al. The identification and management of interstitial lung disease in systemic sclerosis: evidence-based European consensus statements. The Lancet Rheumatology. 2020b;2: e71–e83.
- Asano Y, Jinnin M, Kawaguchi Y, et al. Diagnostic criteria, severity classification and guidelines of systemic sclerosis: Guideline of SSc. J Dermatol. 2018;45, 633–691.
- Maher TM, Molina-Molina M, Russell AM, et al. Unmet needs in the treatment of idiopathic pulmonary fibrosis-insights from patient chart review in five European countries. BMC Pulm Med. 2017;17(1):124.
- Robalo-Cordeiro C, Campos P, Carvalho L, et al. Idiopathic pulmonary fibrosis in the era of antifibrotic therapy: Searching for new opportunities grounded in evidence. Rev Port Pneumol. 2017;23(5):287–293.