Cazuri clinice de pacienți cu PID
PID cu fenotip fibrozant progresiv la pacienți precum Dorina, Luiza și Simion necesită o atenție sporită

Explorați cazurile clinice tipice de PID cu fenotip fibrozant progresiv și impactul acestora asupra pacienților




|
S-O CUNOAȘTEM PE DORINA*
Dorina a fost diagnosticată cu pneumonită de hipersensibilitate fibrozantă cronică în urmă cu un an.
Vârsta: 40
Manifestări pulmonare: PH fibrozantă cronică acum 1 an, cu fenotip progresiv
Istoricul de tratament: medicație anti-inflamatorie
În ciuda tratamentului, Dorina a început să piardă în greutate și a suferit din cauza agravării dispneei,1 iar activitățile care obișnuiau să-i facă plăcere, cum ar fi înotul, au devenit dificile.
„De la diagnosticul meu legat de boala pulmonară, am observat că lipsa de aer s-a agravat. Nu-mi place ca prietenii mei să mă vadă așa, așa că îmi găseam scuze pentru a nu ieși.”
Se prevede că pacienții cu PH fibrozantă cronică, cum ar fi Dorina, vor avea o scădere procentuală semnificativă a FVC, comparativ cu pacienții cu PH fără fibroză (HR=0,22; 95% CI=0,10, 0,51; p<0,001)2
Pacienții cu PH cu fibroză pulmonară fără aspect de fagure de miere au o supraviețuire medie estimată de peste 7,95 ani, comparativ cu 2,76 ani la pacienții cu PH cu aspect de fibroză în fagure de miere2


La pacienții cu PH fibrozantă cronică, o scădere procentuală a CVF de ≥10% din valoarea prezisă în primele 6-12 luni după diagnostic este asociată cu o mortalitate crescută indiferent de cauză1
CÂT TIMP POT SĂ SUPRAVIEȚUIASCĂ PACIENȚII PRECUM DORINA?
Estimările privind supraviețuirea bazată pe modelul Cox în funcție de diagnosticul clinic și grupul de fenotip radiologic2
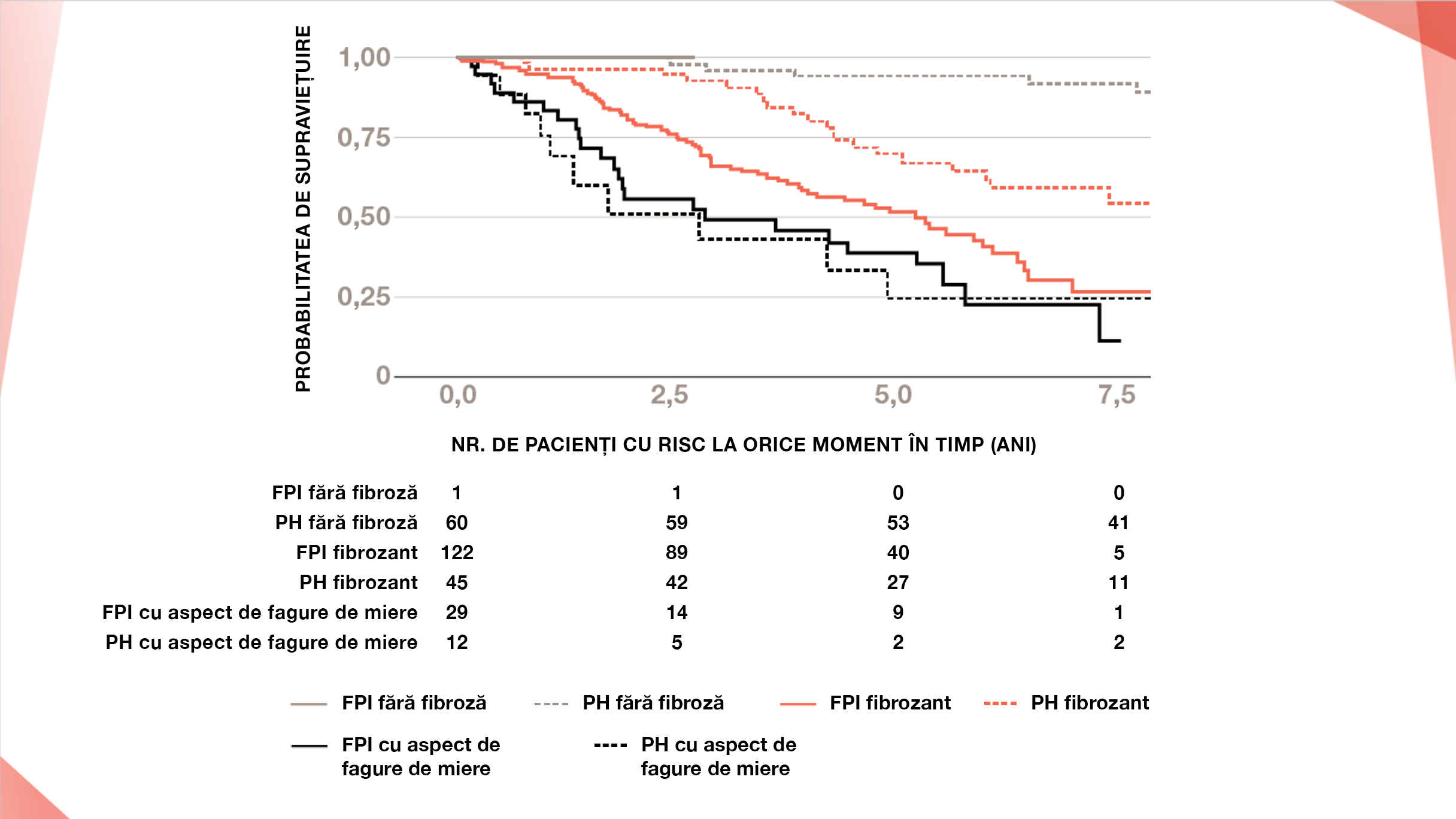
Adaptat după Sailsbury ML, et al. Chest. 2019;155(4):699–711.
Supraviețuirea Kaplan-Meier la pacienții tratați cu corticosteroizi cu PH fibrozantă față de pacienții netratați niciodată4†
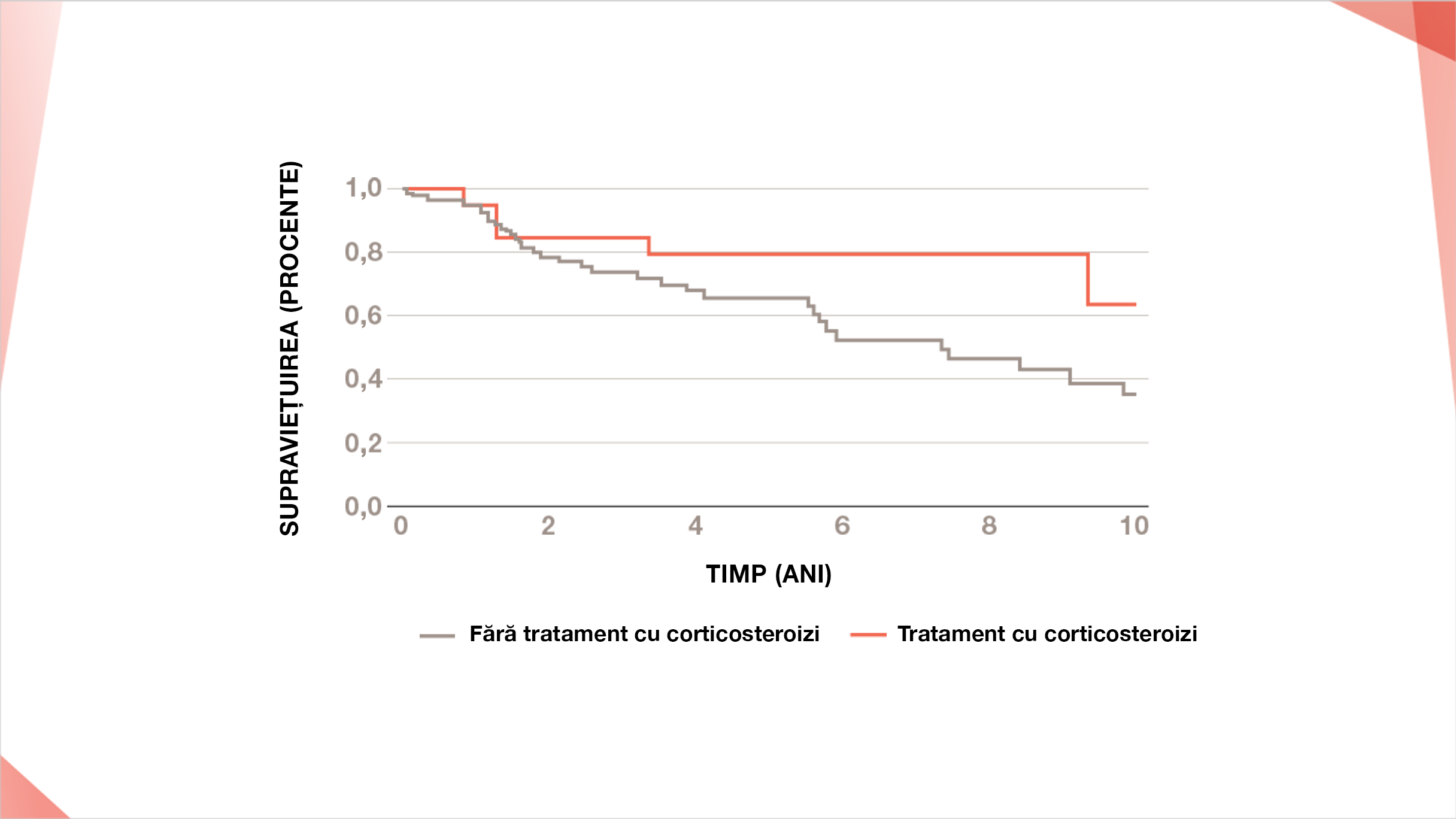
Adaptat după De Sadeleer LJ, et al. J Clin Med. 2018;8(1):pii:E14
† Utilizarea corticosteroizilor la pacienții cu PH cu fenotip fibrozant progresiv a determinat o tendință de supraviețuire mai scăzută (HR=2,2; p=0,096)

Exacerbarea acută a PID este un eveniment grav la pacienții cu PH cronică cu fenotip fibrozant
La pacienții cu PH cronică fibrozantă, la 75% până la 100% dintre pacienții internați pentru o exacerbare acută a PID survine decesul în cursul spitalizării.5
Note
-
*
Pacient ipotetic. Citatele aferente pacienților sunt doar cu titlu demonstrativ.
-
†
Estimările privind procentul de pacienți cu PID non-FPI care dezvoltă fibroză progresivă se bazează pe un sondaj online desfășurat pe 486 de medici (243 de pneumologi, 203 de reumatologi și 40 de interniști) din Statele Unite, Japonia, Franța, Germania, Italia, Spania și Marea Britanie.3

|
S-O CUNOAȘTEM PE LUIZA*
Luiza a fost diagnosticată cu pneumopatie interstițială difuză asociată sarcoidozei în urmă cu un an.
Vârsta: 55
Diagnosticul de bază: Sarcoidoză acum 6 ani
Manifestări pulmonare: pneumopatie interstițială difuză cu fenotip fibrozant progresiv asociată sarcoidozei acum 1 an.
Istoricul de tratament: Antiinflamator întrerupt după 6 luni;6,7 medicație antihipertensivă
Luiza a experimentat recent simptome precum dispneea, care se agravează și care o face să se simtă obosită tot timpul.6,7 Nu este încă o simptomatologie debilitantă, dar se agravează permanent.
„Doar plimbatul câinilor mă lasă fără suflare. Îmi fac griji cât timp mai pot continua până când voi lăsa pe altcineva să facă acest lucru. E atât de deprimant să fii așa”
Pacienții care dezvoltă sarcoidoză pulmonară în stadiul IV†, precum Luiza, au rate de deces mai mari decât populația generală, 75% din mortalitate fiind de cauză respiratorie.6

Fenotipul fibrozant progresiv de pneumopatie interstițială difuză se dezvoltă la aproximativ 20% dintre pacienții cu pneumopatie interstițială difuză asociată cu sarcoidoză3‡
CÂT TIMP POT SUPRAVIEȚUI PACIENȚII PRECUM LUIZA?
Supraviețuirea la pacienții cu sarcoidoză pulmonară în stadiul IV față de populația generală similară din Franța (n=142)6
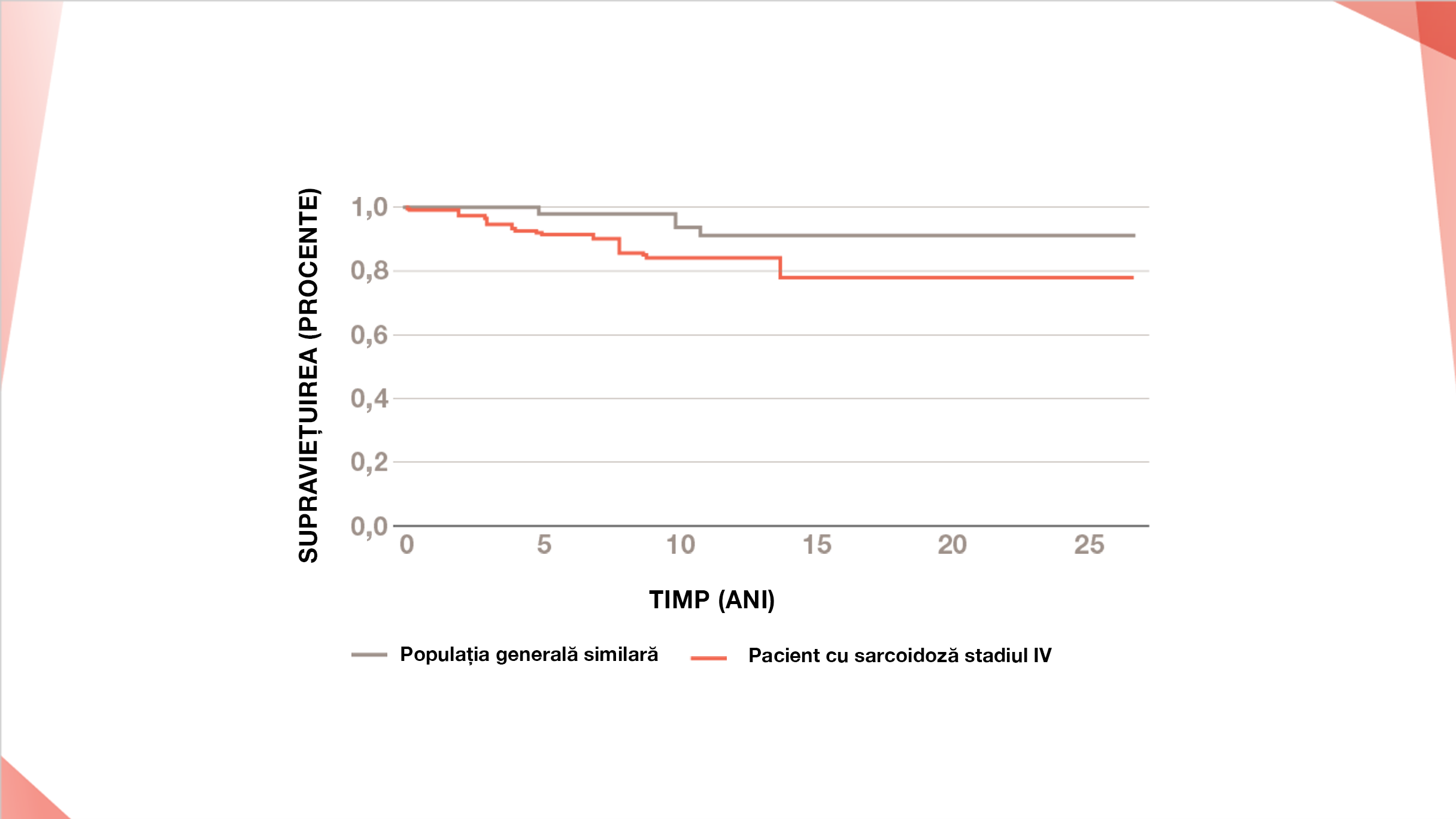
Adaptat după Nardi A, et al. Eur Respir J. 2011;38:1368–1373
CARE ESTE IMPACTUL EXACERBĂRII ACUTE A PID CU FENOTIP FIBROZANT PROGRESIV ÎN CAZUL PACIENȚILOR PRECUM LUIZA?
Agravarea acut㧠a sarcoidozei pulmonare în cazul pacienţilor cu sarcoidoză fibrotică este un eveniment grav şi poate duce la valori semnificative de morbiditate de cauză respiratorie.8
73% dintre pacienții (94 din 129) cu sarcoidoză cu fenotip fibrozant au raportat două sau mai multe evenimente acute de agravare a simptomatologiei în ultimul an8
Note
-
*
Pacient ipotetic. Citatele aferente pacienților sunt doar cu titlu demonstrativ.
-
†
Cu dovezi de pierdere de volum a lobului superior cu retracție hilară cu sau fără mase tumorale, benzi liniare grosiere, aspect de fagure de miere, bule de emfizem.6
-
‡
Estimările privind procentul de pacienți cu PID non-FPI care dezvoltă fibroză progresivă se bazează pe un sondaj online desfășurat pe 486 de medici (243 de pneumologi, 203 de reumatologi și 40 de interniști) din Statele Unite, Japonia, Franța, Germania, Italia, Spania și Marea Britanie.3
-
§
Cauzele agravării acute a sarcoidozei pulmonare includ agravarea bolii de bază, infecțiile, bronhospasmul acut sau cauzele extrapulmonare.8

|
SĂ-L CUNOAȘTEM PE SIMION*
Simion a fost diagnosticat cu pneumonie interstițială idiopatică nespecifică cu fenotip fibrozant în urmă cu doi ani.
Vârsta: 70 ani
Manifestări pulmonare: PIINS fibrotic acum 2 ani, cu fenotip progresiv
Istoric terapeutic: Antiinflamator; reabilitare pulmonară timp de 3 luni; tratament pentru osteoartrită și sindrom de colon iritabil
În pofida tratamentului, Simion continuă să sufere de agravarea dispneei și de o tuse persistentă, neproductivă, care îl ține treaz pe parcursul nopții.9
„Puteți observa cum oamenii se îndepărtează când tușesc. Ei cred că acest lucru este contagios, ceea ce mă face să îmi fie rușine”
Pacienții precum Simion cu PIINS fibrotic sunt expuși riscului de deces prematur.9
La pacienții cu PIINS, o scădere a CVF, % din valoarea prezisă evaluată la 12 luni este asociată cu o mortalitate crescută determinată de această afecțiune9

La aproximativ 26% dintre pacienții cu PIINS survine decesul din cauza stării lor în decurs de 5 ani de la diagnostic9
Note
-
*
Pacient ipotetic. Citatele aferente pacienților sunt doar cu titlu demonstrativ.
-
†
Estimările privind procentul de pacienți cu PID non-FPI care dezvoltă fibroză progresivă se bazează pe un sondaj online desfășurat pe 486 de medici (243 de pneumologi, 203 de reumatologi și 40 de interniști) din Statele Unite, Japonia, Franța, Germania, Italia, Spania și Marea Britanie.3
Ce putem face pentru a ne ajuta pacienții precum Dorina, Luiza și Simion?
Monitorizare precoce și regulată

Intervențiile în cazul PID

Acordarea îngrijirilor paliative/suportive
- Gimenez A, Storrer K, Kuranishi L, et al. Change in FVC and survival in chronic fibrotic hypersensitivity pneumonitis. Thorax. 2018;73:391–392.
- Salisbury ML, Gu T, Murray S, et al. Hypersensitivity pneumonitis: radiologic phenotypes are associated with distinct survival time and pulmonary function trajectory. Chest. 2019;155(4):699–711.
- Wijsenbeek M, Kreuter M, Olson A, et al. Progressive fibrosing interstitial lung diseases: current practice in diagnosis and management. Curr Med Res Opin. 2019:35(11):2015–2024.
- De Sadeleer LJ, Hermans F, De Dycker E, et al. Effects of corticosteroid treatment and antigen avoidance in a large hypersensitivity pneumonitis cohort: a single-centre cohort study. J Clin Med. 2018;8(1):pII:E14.
- Kolb M, Bondue B, Pesci A, et al. Acute exacerbations of progressive-fibrosing interstitial lung diseases. Eur Respir Rev. 2018;27(150):pii:180071.
- Nardi A, Brillet P-Y, Letoumelin P, et al. Stage IV sarcoidosis: comparison of survival with the general population and causes of death. Eur Respir J. 2011;38:1368–1373.
- American Thoracic Society. Statement on Sarcoidosis. Am J Respir Crit Care Med. 1999;160:736–755.
- Baughman RP, Lower EE. Frequency of acute worsening events in fibrotic pulmonary sarcoidosis patients. Respiratory Medicine. 2013;107:2009e2013.
- Park IN, Jegal Y, Kim DS, et al. Clinical course and lung function change of idiopathic nonspecific interstitial pneumonia. Eur Respir J. 2009;33:68–76.
- Cottin V, Hirani N, Hotchkin D, et al. Presentation, diagnosis and clinical course of the spectrum of progressive-fibrosing interstitial lung diseases. Eur Respir Rev. 2018;27(150):180076. N, Jegal Y, Kim DS, et al. Clinical course and lung function change of idiopathic nonspecific interstitial pneumonia. Eur Respir J. 2009;33:68–76.
- Maher TM, Molina-Molina M, Russell AM, et al. Unmet needs in the treatment of idiopathic pulmonary fibrosis-insights from patient chart review in five European countries. BMC Pulm Med. 2017;17(1):124.
- Molina-Molina M, Aburto M, Acosta O, et al. Importance of early diagnosis and treatment in idiopathic pulmonary fibrosis. Exp Rev Resp Med. 2018;12(7):537–539.
- Robalo-Cordeiro C, Campos P, Carvalho L, et al. Idiopathic pulmonary fibrosis in the era of antifibrotic therapy: Searching for new opportunities grounded in evidence. Rev Port Pneumol. 2017;23(5):287–293.
- Ryerson CJ, Cayou C, Topp F, et al. Pulmonary rehabilitation improves long-term outcomes in interstitial lung disease: a prospective cohort study. Respir Med. 2014;108(1):203-210.
- Kreuter M, Bendstrup E, Russell A, et al. Palliative care in interstitial lung disease: living well. Lancet Respir Med. 2017;5(12):968-980.
- Maher TM, Wuyts W. Management of Fibrosing Interstitial Lung Diseases. Adv Ther. 2019;doi:10.1007/s12325-019-00992-9. [Epub ahead of print].
- Sgalla G, Cerri S, Ferrari R, et al. Mindfulness-based stress reduction in patients with interstitial lung diseases: a pilot, single-centre observational study on safety and efficacy. BMJ Open Respir Res. 2015;2(1):e000065.
