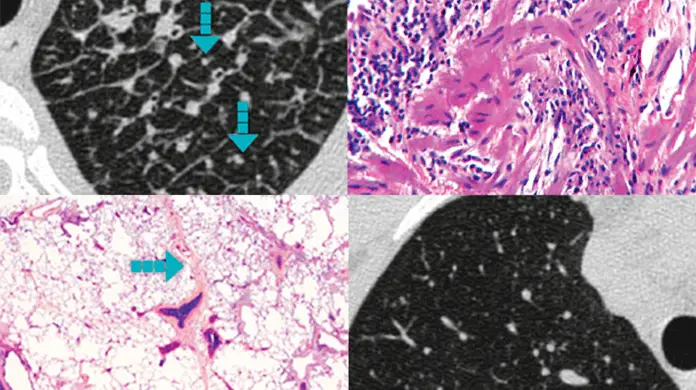
Imagistica HRCT în cazul fibrozei pulmonare
HRCT este instrumentul de diagnostic neinvaziv, standardul de aur pentru PID cu fenotip fibrozant1,2

Tomografia computerizată de înaltă rezoluție (HRCT) este esențială pentru a ajunge la diagnostice precise de fibroză pulmonară în PID, precum și pentru evaluarea leziunilor, monitorizarea modificărilor, screening-ul pentru complicații și evaluarea prognosticului.3
Heterogenitatea și imprevizibilitatea PID pot face ca fibroza pulmonară să reprezinte o provocare de diagnostic, ducând adesea la un diagnostic întârziat.4–7
IMAGINILE HRCT VĂ AJUTĂ SĂ RECUNOAȘTEȚI PID CU FENOTIP FIBROZANT
ASPECT DE FAGURE DE MIERE
Caracteristici
Spații aeriene chistice grupate, cu pereți bine delimitați, măsurând 2–10 mm în diametru, ajungând uneori la 25 mm, de obicei în regiunile subpleurale
Semne asociate cu aspectul de fagure de miere
Reticulații intralobulare
Bronșiectazii de tracțiune și bronșiectazii
Pierderea în volum a lobului pulmonar
Distorsiunea scizurii pulmonare
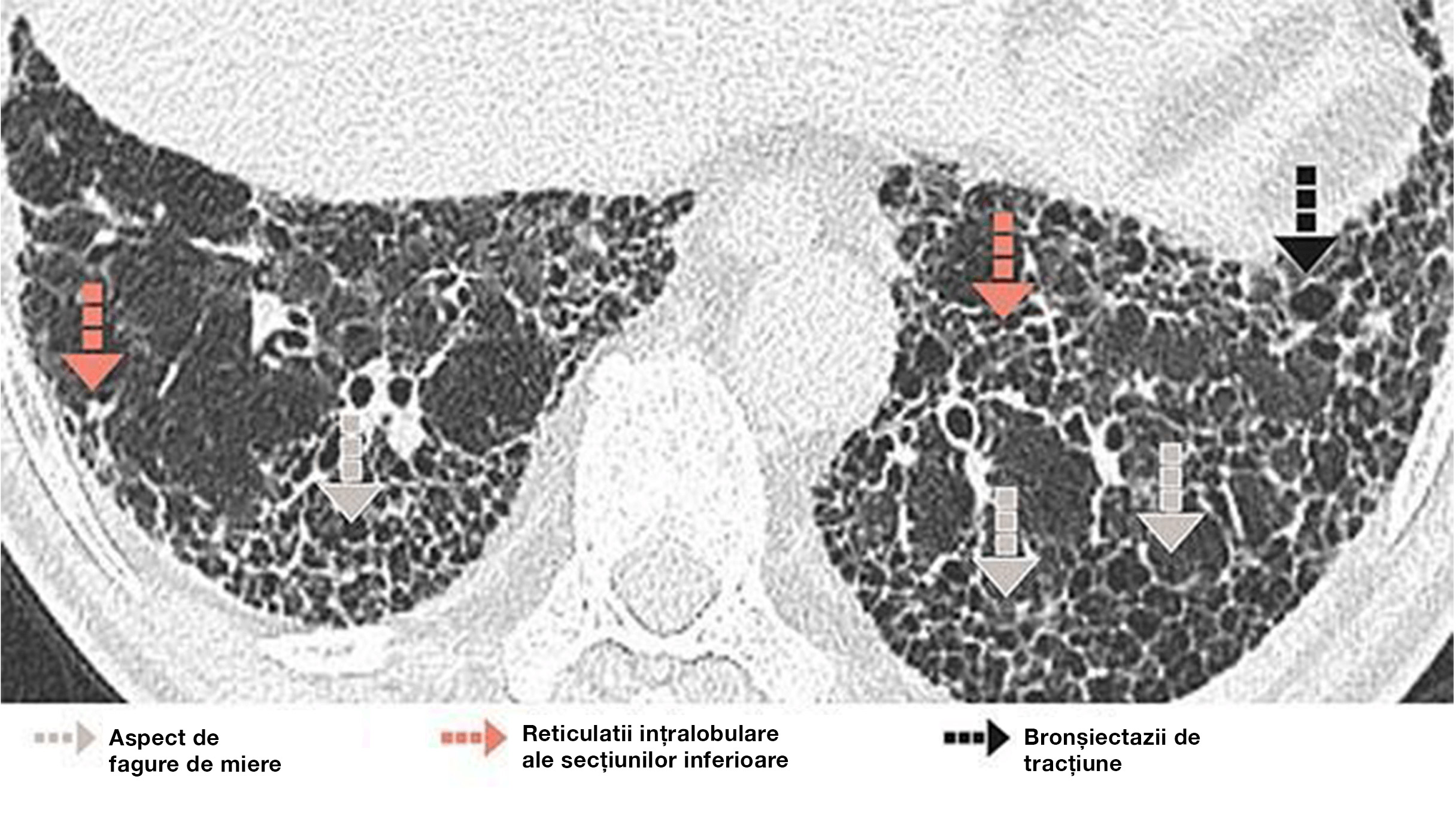
|
Aspect de fagure de miere subpleural care formează mai multe straturi de chisturi la un bărbat de 73 de ani cu UIP
BRONȘIECTAZII DE TRACȚIUNE / BRONHIOLECTAZII
Caracteristici
Dilatarea anormală și neregulată a bronhiilor/bronhiolelor din cauza inflamației tractului respirator (uneori reversibilă) sau a fibrozei pulmonare
La scanarea HRCT, apare ca o creștere a calibrului tractului respirator distal (fără reducerea diametrului periferic, vizibilă pulmonar subpleural la cel puțin 20 mm de pleură)
La scanare, se prezintă ca spații de aer tubulare sau chistice în funcție de orientarea bronhiilor în secțiune transversală.
Diferențierea între bronșiectaziile de tracțiune și aspectul de fagure de miere este uneori dificilă pe secțiunile transversale axiale. Secțiunile transversale sagitale sau coronale și minIP sunt cele uzuale.
Diagnosticul orientativ
Bronșiectaziile de tracțiune sunt asociate cu semne de fibroză
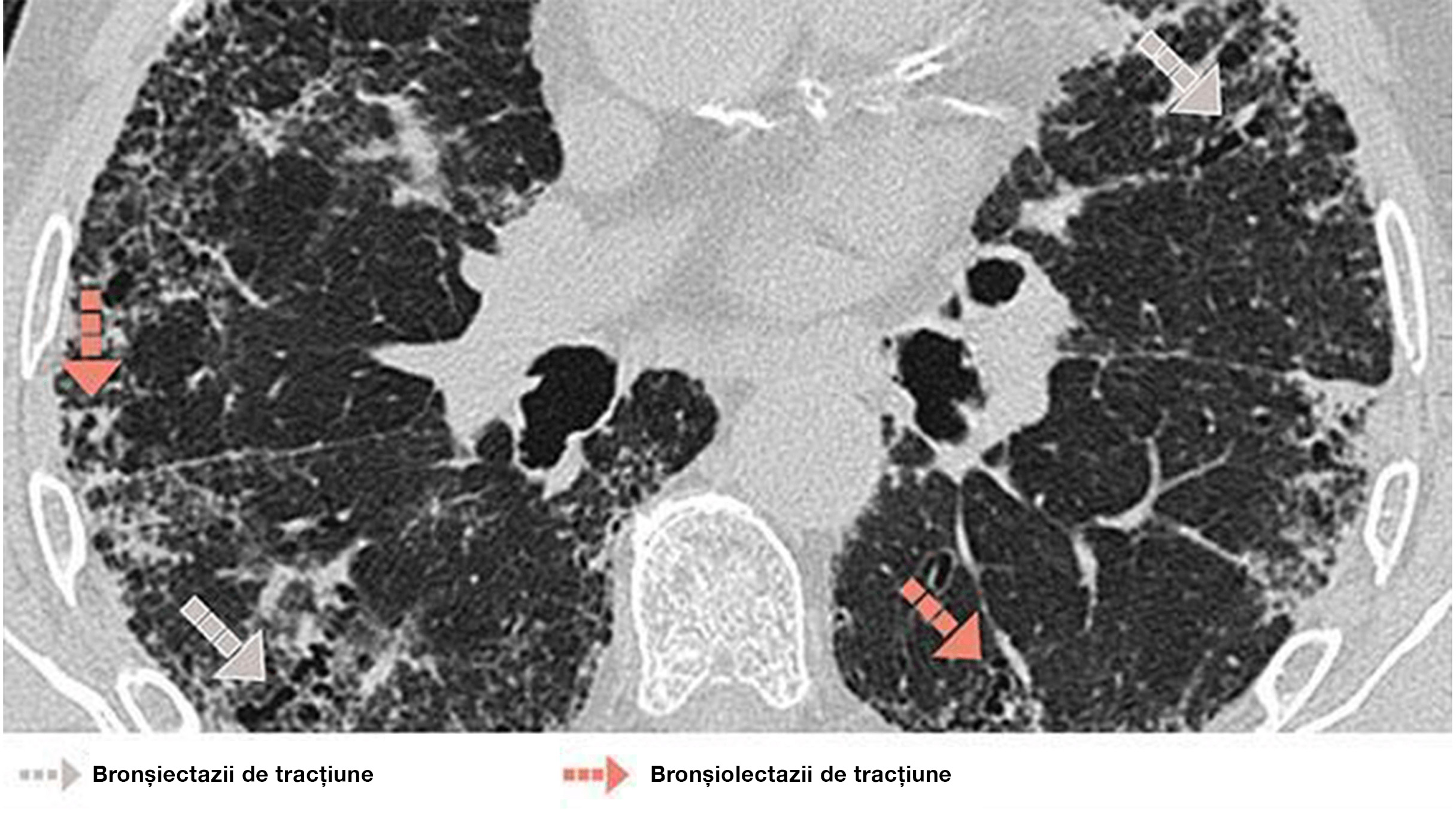
|
Bărbat de 72 de ani cu UIP. HRCT evidențiază reticulații difuze și bronșiolectaze și bronșiectazii de tracțiune.
FPI – MODEL UIP
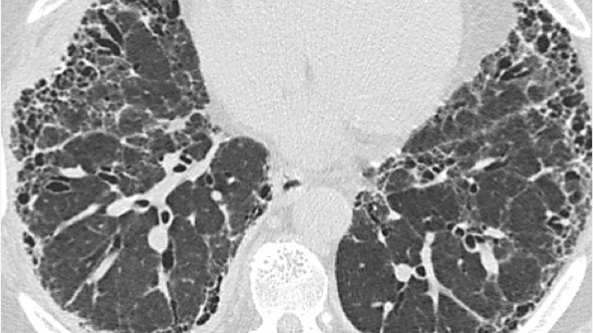
|
Recomandările ATS/ERS/JRS/ALAT menționează că FPI poate fi diagnosticată cu încredere dacă evaluarea clinică a pacientului indică FPI și HRCT arată un model UIP cert sau probabil (recomandare de biopsie condiționată)2
De ce este important screening-ul și diagnosticul precoce al FPI cu ajutorul HRCT?
PHc
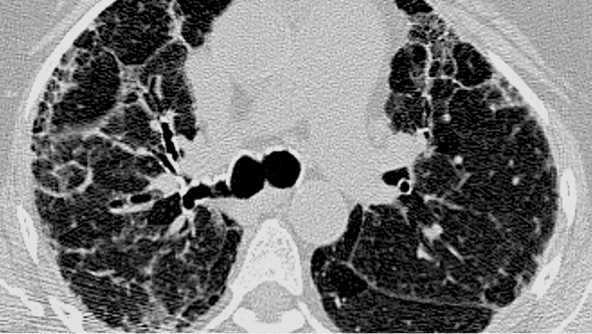
|
Îngroșarea reticulară subpleurală, hiperinflație pulmonară și bronșiectazii de tracțiune
PNEUMOPATIA INTERSTIȚIALĂ DIFUZĂ ASOCIATĂ SARCOIDOZEI
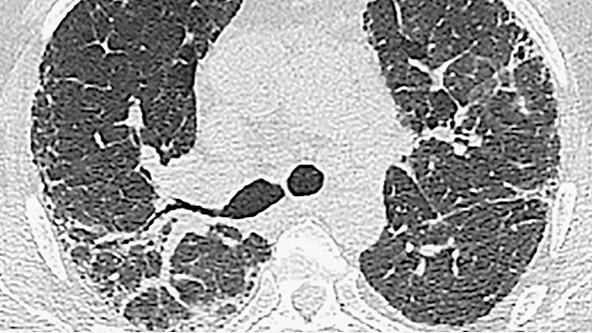
|
Cum sunt afectați pacienții de pneumopatia interstițială difuză asociată cu sarcoidoza?
ASPECT PIINS - NSIP
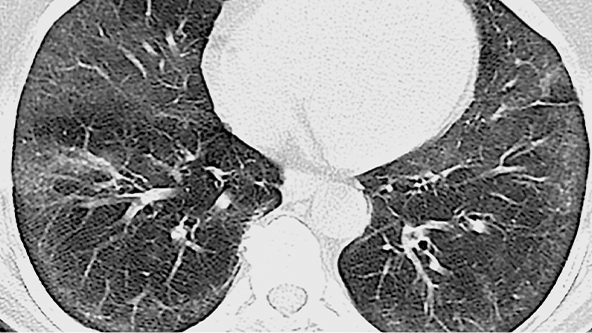
|
Opacități cu aspect de sticlă mată, cruțare subpleurală și bronșiectazii de tracțiune
Aflați mai multe despre modul în care iNSIP poate afecta viața pacienților dvs.
Interpretarea corectă a HRCT este esențială pentru a ajuta la sprijinirea pacienților cu PID cu fenotip fibrozant progresiv

Evaluarea inițială a PID
Diagnosticul PID

Cazuri de pacienți cu PID pentru evaluare și diagnostic
Note
ALAT, Societatea Toracică Latino-Americană; ATS, Societatea Toracică Americană; ERS, Societatea Europeană de Respirație; HRCT, tomografie computerizată de înaltă rezoluție; BPI, boală pulmonară interstițială; PIINS, pneumonie interstițială nespecifică idiopatică; FPI, fibroză pulmonară idiopatică; JRS, Societatea Respiratorie Japoneză; UIP, pneumonie interstițială obișnuită.
- Chowaniec M, Skoczyńska M, Sokolik R, Wiland P. Interstitial lung disease in systemic sclerosis: challenges in early diagnosis and management. Reumatologia. 2018;56(4):249–254.
- Raghu G, Remy-Jardin M, Myers JL, et al; on behalf of the ATS/ERS/JRS/ALAT. Diagnosis of Idiopathic Pulmonary Fibrosis. An Official ATS/ERS/JRS/ALAT Clinical Practice Guideline. Am J Respir Crit Care Med. 2018;198(5):e44–e68.
- Brauner M, et al. Imagerie des pneumopathies infiltrantes diffuses. Press Med. 2010;39:73–84.
- Wells AU, Brown KK, Flaherty KR, et al. What’s in a name? That which we call IPF, by any other name would act the same. Eur Respir J. 2018;51(5):1800692.
- Wijsenbeek MS, Kreuter M, Olson A, et al. Progressive fibrosing interstitial lung diseases: current practice in diagnosis and management. Curr Med Res Opin. 2019:1–10.
- Gulati M. Diagnostic assessment of patients with interstitial lung disease. Prim Care Respir J. 2011;20:120–127.
- Greiffo FR, Eickelberg O, Fernandez IE. Systems medicine advances in interstitial lung disease. Eur Respir Rev. 2017;26:170021.
- Chaudhuri N, Spencer L, Greaves M, et al. A Review of the Multidisciplinary Diagnosis of Interstitial Lung Diseases: A Retrospective Analysis in a Single UK Specialist Centre. J Clin Med. 2016;5(66):1–9.
- Cottin V, Hirani N, Hotchkin D, et al. Presentation, diagnosis and clinical course of the spectrum of progressive-fibrosing interstitial lung diseases. Eur Respir Rev. 2018;27(150):180076.
- Cottin V, Brown KK. Interstitial lung disease associated with systemic sclerosis (SSc–ILD). Respir Res. 2019a;20(1):13.
- Wong AW, Ryerson C, Guler S. Progression of fibrosing interstitial lung disease. Respir Res. 2020:29;21(1):32.
- Flaherty KR, Brown KK, Wells AU, et al. Design of the PF-ILD trial: A double-blind, randomised, placebo-controlled phase III trial of nintedanib in patients with progressive fibrosing interstitial lung disease. BMJ Open Resp Res. 2017;4(1):e000212.
- Theodore AC, Tseng C-H, Li N, Elashoff RM, Tashkin DP. Correlation of cough with disease activity and treatment with cyclophosphamide in scleroderma interstitial lung disease: findings from the Scleroderma Lung Study. Chest. 2012;142(3):614–621.
- Hoffmann-Vold AM, Fretheim H, Halse AK, et al. Tracking impact of interstitial lung disease in systemic sclerosis in a complete nationwide cohort. Am J Respir Crit Care Med. 2019;200:1258–1266.
- Hoffmann-Vold AM, Maher TM, Philpot EE, et al. The identification and management of interstitial lung disease in systemic sclerosis: evidence-based European consensus statements. The Lancet Rheumatology. 2020b;2: e71–e83.
- Asano Y, Jinnin M, Kawaguchi Y, et al. Diagnostic criteria, severity classification and guidelines of systemic sclerosis: Guideline of SSc. J Dermatol. 2018;45, 633–691.