Screeningul
PID în AR
Pacienții cu poliartrită reumatoidă (AR) cu factori de risc pentru pneumopatia interstițială difuză (PID) sau simptome pulmonare trebuie evaluați pentru PID la diagnosticul inițial de AR1,2

FACTORII DE RISC PENTRU DEZVOLTAREA PID TREBUIE EVALUAȚI ODATĂ CU STABILIREA DIAGNOSTICULUI INIȚIAL DE AR1,2
Factori de risc pentru dezvoltarea PID la pacienții cu AR | |
|---|---|
Vârsta |
|
Sex |
|
Stilul de viață |
|
Serologie | |
Clinic | |
În ciuda faptului că PID-AR este frecventă la pacienții cu vârsta cuprinsă între 40 și 50 de ani, pacienții cu vârsta > 60 de ani prezintă un risc crescut de a dezvolta PID5,7
Pentru fiecare creștere cu 10 ani a intervalului de vârstă, probabilitatea de a dezvolta PID crește cu 64%15
PID-AR este de aproximativ de patru ori mai frecventă la bărbați decât la femei.1,8
Fumatul crește riscul de PID la pacienții cu AR6,9, dar este important de menționat că PID-AR poate apărea și la nefumători.19
Serologiile pozitive pentru anticorpi RF sau anti-CCP sunt predictori semnificativi pentru dezvoltarea PID la pacienții cu AR6,10–14.
PACIENȚII AR CU FACTORI DE RISC PENTRU PID SAU SIMPTOME PULMONARE PRE-EXISTENTE LA DIAGNOSTICUL DE BAZĂ AL AR TREBUIE EVALUAȚI PENTRU PID1,2
Evaluarea prentru PID folosind PFR la momentul inițial și HRCT este rezonabilă pentru a identifica PID în AR1
Un istoric de fumat la un pacient cu PID-AR ar trebui să conducă la investigații cu o radiografie toracică și spirometrie în primă instanță20
Identificarea ralurilor la auscultația pulmonară poate fi un instrument util pentru a evidenția PID subclinic la pacienții cu AR, invitând evaluarea completă a funcției pulmonare20,21.
Algoritm sugerat pentru identificarea PID-AR la pacienții cu AR1
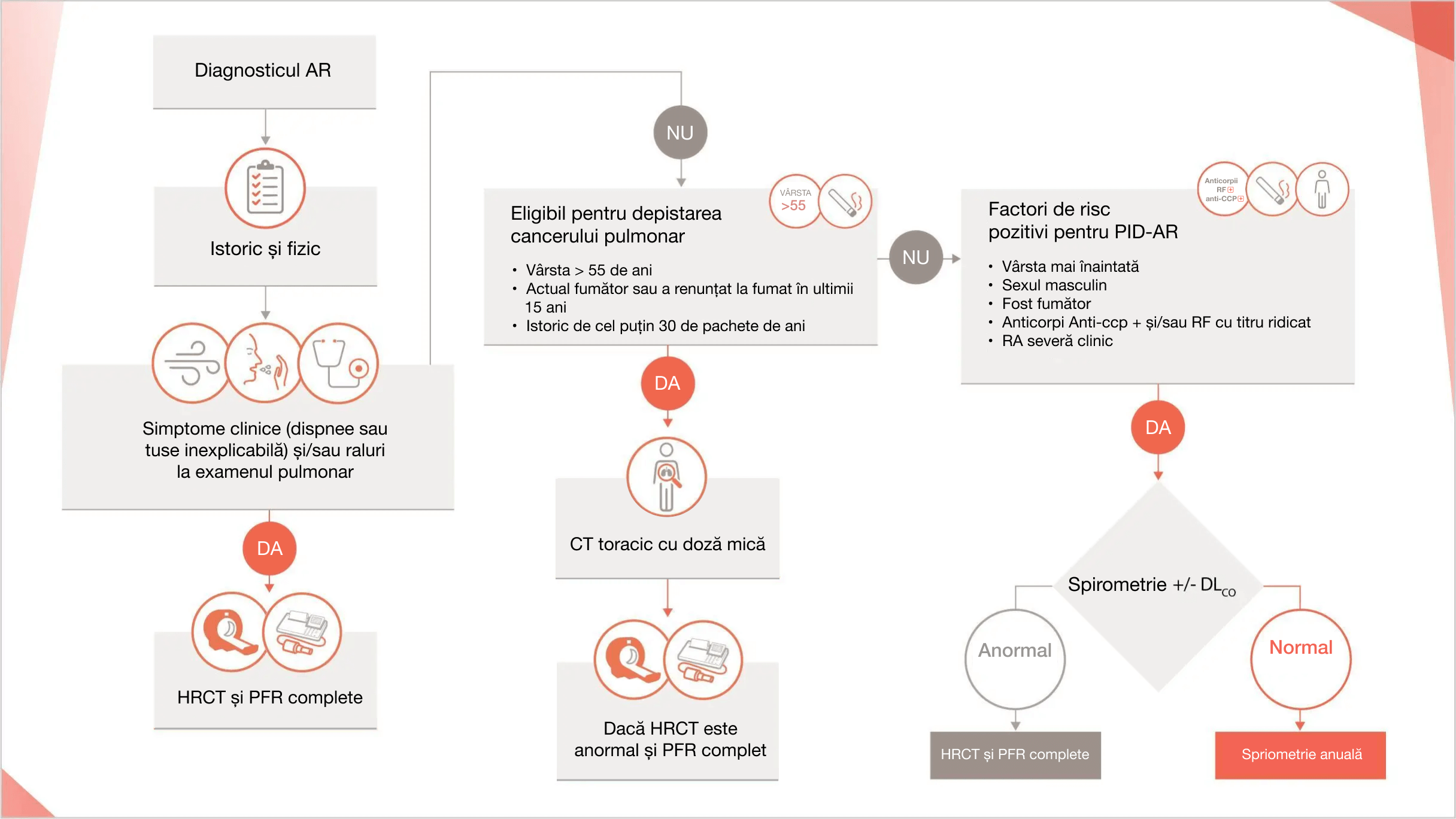
Retipărit după Clinics in Chest Medicine, 40(3), Esposito et al, Thoracic Manifestations of Rheumatoid Arthritis, 545-560, ©2022, cu permisiunea Elsevier.
Iulia are PID-AR
Cum poți ajunge la un diagnostic PID-AR?
Odată ce ați ajuns la un diagnostic, cum ar trebui să faceți managementul pacienților cu PID-AR?
Monitorizarea și managementul progresiei PID în PID-AR

Oferirea de îngrijiri paliative/ de susținere
Echipa multidisciplinară
Note
-
CCP, peptidă citrulinată ciclică; CT, tomografie computerizată; PID-BTC, pneumopatie interstițială difuză asociată cu boli ale țesutului conjunctiv; DLCO, factorul de transfer gazos pentru monoxid de carbon; VSH, viteza de sedimentare a eritrocitelor; HRCT, tomografie computerizată de înaltă rezoluție; PID pneumopatie interstițială difuză; KL-6, Krebs von den Lungen-6; PFR, probe funcționale respiratorii; AR; artrita reumatoidă; PID-AR, pneumopatie interstițială difuză asociată cu artrita reumatoidă; RF, factor reumatoid.
- Esposito AJ, Chu SG, Madan R, et al. Thoracic manifestations of rheumatoid arthritis. Clin Chest Med. 2019;40(3):545–560.
- Wallace B, Vummidi D, Khanna D. Management of connective tissue diseases associated interstitial lung disease: a review of the published literature. Curr Opin Rheumatol. 2016;28(3):236–245.
- Olson AL, Swigris JJ, Sprunger DB, et al. Rheumatoid arthritis-interstitial lung disease associated mortality. Am J Respir Crit Care Med. 2011;183(3):372-378.
- Geerts S, Wuyts W, De Langhe E, et al. Connective tissue disease associated interstitial pneumonia: a challenge for both rheumatologists and pulmonologists. Sarcoidosis Vasc Diffuse Lung Dis. 2017;34(4):326–335.
- Shaw M, Collins BF, Ho LA, Raghu G. Rheumatoid arthritis-associated lung disease. Eur Respir Rev. 2015;24(135):1–16.
- Kelly CA, Saravanan V, Nisar M, et al. Rheumatoid arthritis-related interstitial lung disease: associations, prognostic factors and physiological and radiological characteristics – a large multicentre UK study. Rheumatology (Oxford). 2014;53(9):1676–1682.
- Brito Y, Glassberg MK, Ascherman DP. Rheumatoid Arthritis-Associated Interstitial Lung Disease: Current Concepts. Curr Rheumatol Rep. 2017;19:79. doi: 10.1007/s11926-017-0701-5.
- Koo SM, Kim SY, Choi SM, et al. Korean guidelines for diagnosis and management of interstitial lung diseases: part 5. Connective tissue disease associated interstitial lung disease. Tuberc Respir Dis (Seoul). 2019;82(4):285–297.
- Gochuico BR, Avila NA, Chow CK, et al. Progressive preclinical interstitial lung disease in rheumatoid arthritis. Arch Intern Med. 2008;168(2):159–166.
- Mori S, Koga Y, Sugimoto M. Different risk factors between interstitial lung disease and airway disease in rheumatoid arthritis. Respir Med. 2012;106(11):1591–1599.
- Habib HM, Eisa AA, Arafat WR, et al. Pulmonary involvement in early rheumatoid arthritis patients. Clin Rheumatol. 2011;30:217–221.
- Doyle TJ, Patel AS, Hatabu H, et al. Detection of rheumatoid arthritis–interstitial lung disease is enhanced by serum biomarkers. Am J Respir Crit Care Med. 2015;191(12):1403–1412.
- Giles JT, Danoff SK, Sokolove J, et al. Association of fine specificity and repertoire expansion of anticitrullinated peptide antibodies with rheumatoid arthritis associated interstitial lung disease. Ann Rheum Dis. 2014;73:1487–1494.
- Yin Y, Liang D, Zhao L, et al. Anti-cyclic citrullinated Peptide antibody is associated with interstitial lung disease in patients with rheumatoid arthritis. PLoS One. 2014;9(4):e92449.
- Koduri G, Norton S, Young A, et al. Interstitial lung disease has a poor prognosis in rheumatoid arthritis: results from an inception cohort. Rheumatology (Oxford). 2010; 49(8):1483–1489.
- Avouac J, Cauvet A, Steelandt A, et al. Improving risk-stratification of rheumatoid arthritis patients for interstitial lung disease. PLoS One. 2020;15(5):e0232978. doi:10.1371/journal.pone.0232978.
- Ha YJ, Lee YJ, Kang EH. Lung involvements in rheumatic diseases: update on the epidemiology, pathogenesis, clinical features, and treatment. Biomed Res Int. 2018:6930297.
- Bongartz T, Nannini C, Medina-Velasquez YF, et al. Incidence and mortality of interstitial lung disease in rheumatoid arthritis: a population-based study. Arthritis Rheum. 2010;62(6):1583–1591.
- Ayhan-Ardic FF, Oken O, Yorgancioglu ZR, et al. Pulmonary involvement in lifelong non-smoking patients with rheumatoid arthritis and ankylosing spondylitis without respiratory symptoms. Clin Rheumatol. 2006;24:213–218.
- Lake F and Proudman S. Rheumatoid arthritis and lung disease: from mechanisms to a practical approach. Semin Respir Crit Care Med. 2014;35(2):222–238.
- Cottin V and Cordier JF. Subclinical interstitial lung disease: no place for crackles? Am J Respir Crit Care Med. 2012;186(3):289–290.
- Iqbal K and Kelly C. Treatment of rheumatoid arthritis-associated interstitial lung disease: a perspective review. Ther Adv Musculoskelet Dis. 2015;7(6):247–267.
- Cassone G, Manfredi A, Vacchi C, et al. Treatment of rheumatoid arthritis-associated interstitial lung disease: lights and shadows. J Clin Med. 2020;9(4):1082. doi: 10.3390/jcm9041082.
- Ryerson CJ, Cayou C, Topp F, et al. Pulmonary rehabilitation improves long-term outcomes in interstitial lung disease: a prospective cohort study. Respir Med. 2014;108(1):203-210.
- Kreuter M, Bendstrup E, Russell A, et al. Palliative care in interstitial lung disease: living well. Lancet Respir Med. 2017;5(12):968-980.
- Maher TM, Wuyts W. Management of Fibrosing Interstitial Lung Diseases. Adv Ther. 2019;doi:10.1007/s12325-019-00992-9. [Epub ahead of print].
- Sgalla G, Cerri S, Ferrari R, et al. Mindfulness-based stress reduction in patients with interstitial lung diseases: a pilot, single-centre observational study on safety and efficacy. BMJ Open Respir Res. 2015;2(1):e000065.
- Wijsenbeek M, Cottin V. Spectrum of Fibrotic Lung Diseases. N Engl J Med. 2020;383:958–968.
