Interacțiunea dintre inflamație și fibroză în PID-BTC
Indiferent de declanșarea leziunii pulmonare, pneumopatiile interstițiale difuze fibrozante cronice asociate cu boli ale țesutului conjunctiv (PID-BTC) prezintă aspecte comune în mecanismele patogenice care generează fibroza1-3.

PATOGENEZA PID-BTC IMPLICĂ INTERACȚIUNEA PRECOCE ÎN EVOLUȚIA BOLII DINTRE INFLAMAȚIE ȘI FIBROZĂ4-6
MECANISMELE PATOGENICE COMUNE ALE FIBROZEI PULMONARE ÎN PID-BTC
Aflați despre mecanismele fiziopatologice aplicabile unei game largi de PID-BTC fibrotice care pot dezvolta un fenotip fibrozant progresiv
În timp ce PID sunt diferite, căile patogenice către fibrogeneză sunt comune, independent de factorul declanșator al leziune pulmonare1–3,7
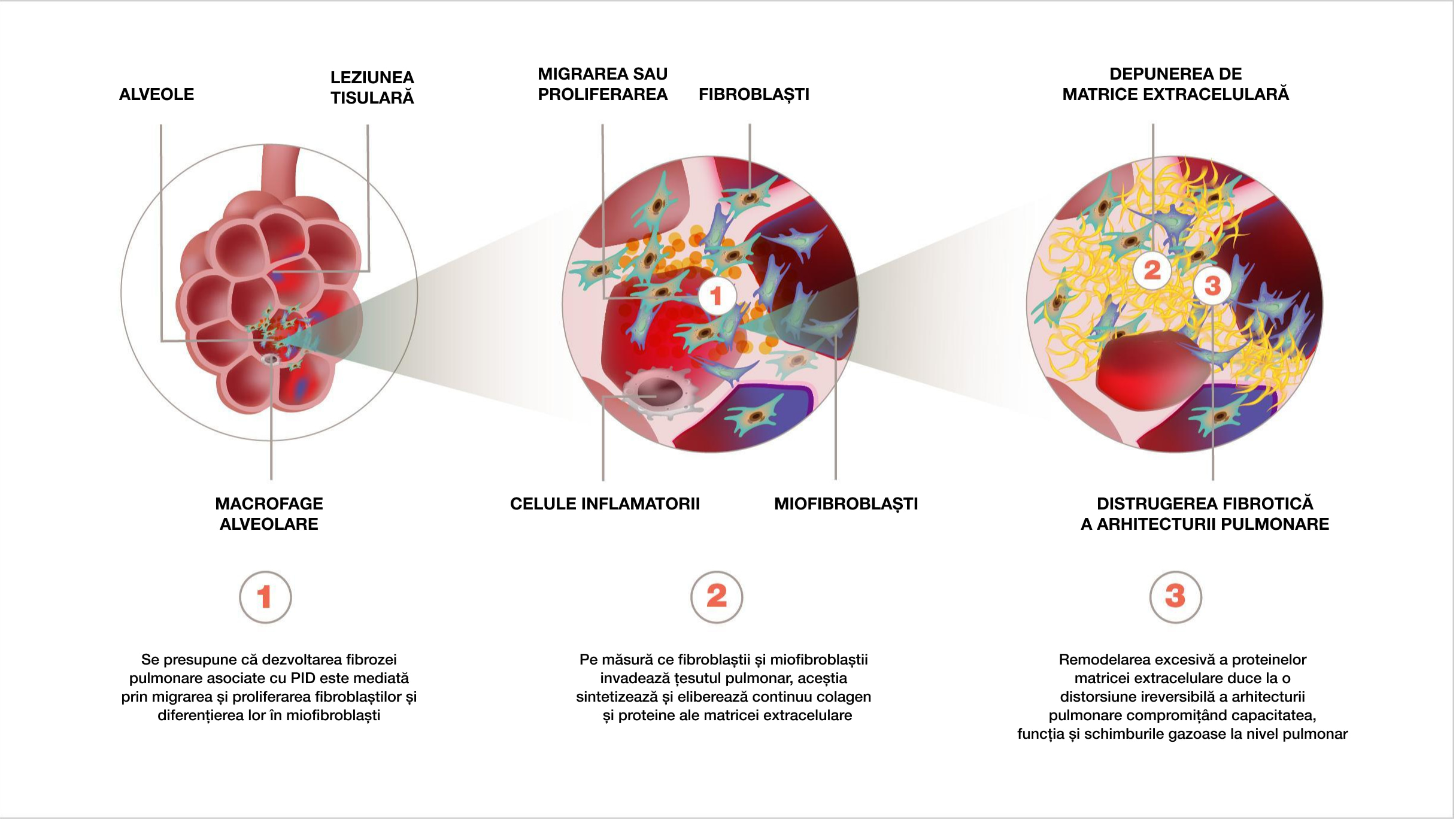
Autoimunitatea și/sau leziunile repetitive ale epiteliului alveolar și/sau endoteliului vascular pot cauza activarea persistentă a fibroblaștilor și leziuni progresive prin intermediul
cercurilor vicioase ale evenimentelor profibrotice4,5,8,9
O interacțiune complexă a proceselor inflamatorii, fibrotice și vasculare duce la activarea și proliferarea fibroblaștilor, diferențierea lor în miofibroblaști și secreția excesivă a matricei extracelulare4,5,10
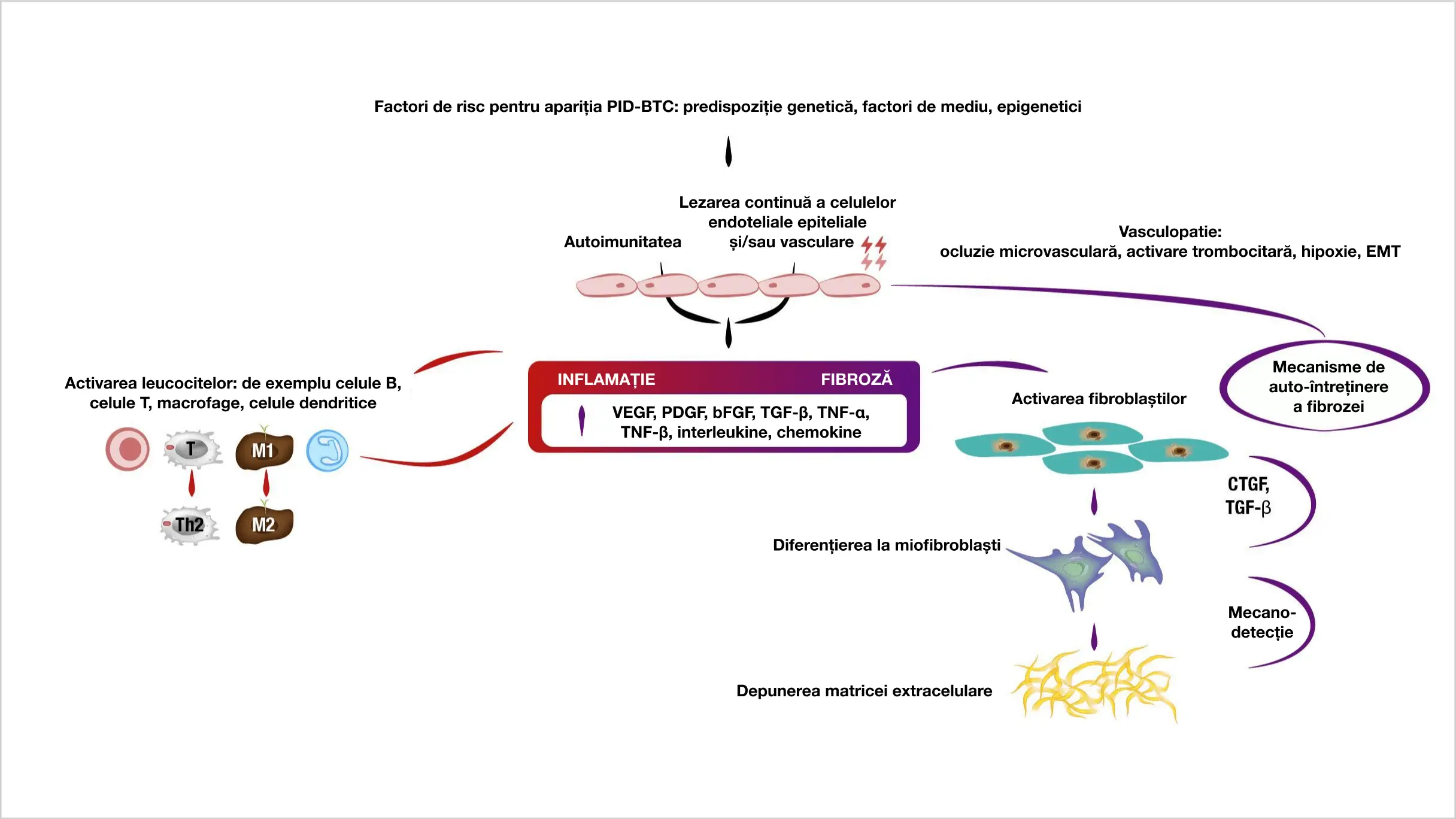
Mecanismele din spatele inflamației și fibrozei în patogeneza PID-BTC4,8–16
Cum puteți identifica PID fibrozantă progresivă cât mai precoce la pacienții dumneavoastră cu BTC?

Screening pentru PID în BTC
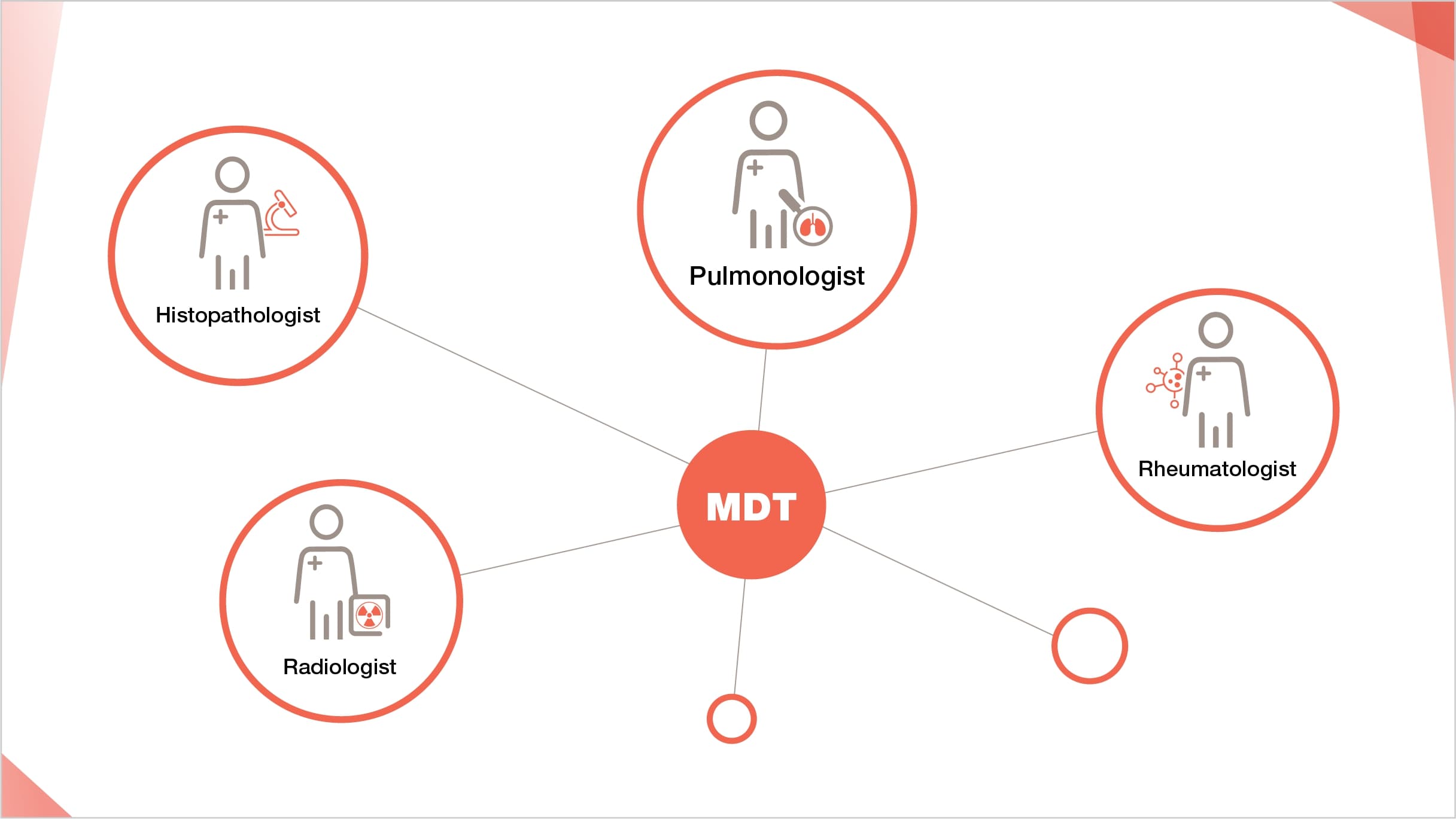
Diagnosticul PID-BTC
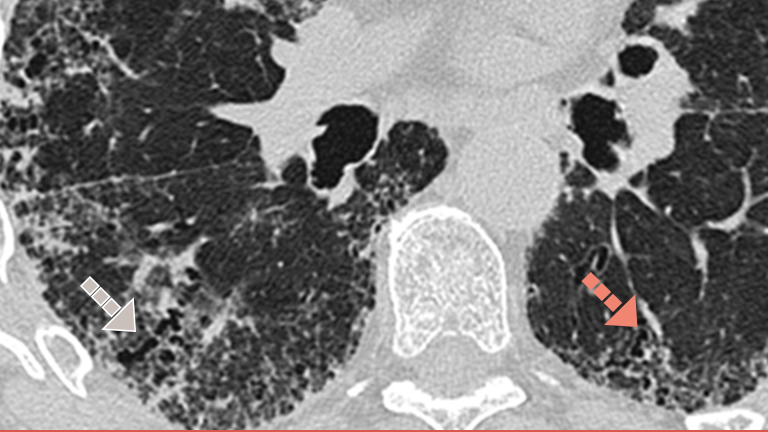
Investigarea PID-BTC fibrozante progresive cu ajutorul imagisticii HRCT
PHc, pneumonită cronică de hipersensibilitate; BTC, boala țesutului conjunctiv; DLCO, capacitatea de difuzie a plămânului pentru monoxid de carbon; PH, pneumonită de hipersensibilitate; HRCT, tomografie computerizată de înaltă rezoluție; BPI, boală pulmonară interstițială; PIINS, pneumopatie interstițială nespecifică idiopatică; FPI, fibroză pulmonară idiopatică; PFR, probe funcționale respiratorii; AR artrită reumatoidă;PID-AR, pneumopatie interstițială difuză asociată artritei reumatoide; ScS, scleroză sistemică; PID-SCS, pneumopatie interstițială difuză asociată sclerozei sistemice.
Note
bFGF, factor bazal de creștere al fibroblaștilor; BTC, boli ale țesutului conjunctiv; PID-BTC, pneumopatie interstițială difuză asociată cu boli ale țesutului conjunctiv; CTGF, factor de creștere al țesutului conjunctiv;
EMT, tranziție epitelial-mezenchimală; HRCT, tomografie computerizată de înaltă rezoluție; PID, pneumopatie interstițială difuză; MMP, metaloproteinaza matricei celulare; PDGF, factor de creștere derivat plachetar;
PFR, probe funcționale respiratorii; TGF-p, factor de creștere transformator-p; TNF-α, factor de necroză tumorală-α; TNF-p, factor de necroză tumorală-p; VEGF, factor de creștere a endoteliului vascular.
- Maher TM, Wuyts W. Management of fibrosing interstitial lung diseases. Adv Ther. 2019;36(7):1518–1531.
- Wuyts WA, Agostini C, Antoniou KM, et al. The pathogenesis of pulmonary fibrosis: a moving target. Eur Respir J. 2013;41(5):1207–1218.
- Kolb M, Vašáková M. The natural history of progressive fibrosing interstitial lung diseases. Respir Res. 2016;20(1).
- Wells AU, Denton CP. Interstitial lung disease in connective tissue disease — mechanisms and management. Nat Rev Rheumatol. 2014;10:728–739.
- Castelino FV and Varga J. Interstitial lung disease in connective tissue diseases: evolving concepts of pathogenesis and management. Arthritis Res Ther. 2010;12(4):213. doi: 10.1186/ar3097.
- Dellaripa PF. Interstitial lung disease in the connective tissue diseases; a paradigm shift in diagnosis and treatment. Clin Immunol. 2018;186:71–73.
- Cottin V, Hirani N, Hotchkin D, et al. Presentation, diagnosis and clinical course of the spectrum of progressive-fibrosing interstitial lung diseases. Eur Respir Rev. 2018;27(150):180076.
- Shaw M, Collins BF, Ho LA, Raghu G. Rheumatoid arthritis-associated lung disease. Eur Respir Rev. 2015;24(135):1–16.
- Cavagna L, Monti S, Grosso V, et al. The multifaceted aspects of interstitial lung disease in rheumatoid arthritis. Biomed Res Int. 2013;2013:759760. doi: 10.1155/2013/759760.
- Fischer A and Distler J. Progressive fibrosing interstitial lung disease associated with systemic autoimmune diseases. Clin Rheumatol. 2019;38(10):2673–2681.
- Cutolo M, Soldano S, Smith V. Pathophysiology of systemic sclerosis: current understanding and new insights. Exp Rev Clin Immunol. 2019;15:753–764.
- Khanna D, Tashkin DP, Denton CP, et al. Etiology, Risk Factors, and Biomarkers in Systemic Sclerosis with Interstitial Lung Disease. Am J Respir Crit Care Med. 2020;201:650–660.
- Volkmann E, Varga J. Emerging targets of disease-modifying therapy for systemic sclerosis. Nat Rev Rheumatol. 2019;15:208–224.
- Varga J, Abraham D. Systemic sclerosis: a prototypic multisystem fibrotic disorder. J Clin Invest. 2007;117:557-567.
- Bagnato G and Harari S. Cellular interactions in the pathogenesis of interstitial lung diseases. Eur Respir Rev. 2015;24(135):102–114. Fischer A and Distler J. Progressive fibrosing interstitial lung disease associated with systemic autoimmune diseases. Clin Rheumatol. 2019;38(10):2673–2681.
- Nicolosi P A, Tombetti E, Maugeri N, et al. Vascular Remodelling and Mesenchymal Transition in Systemic Sclerosis. Stem Cell Int. 2016; doi: 10.1155/2016/4636859.
- Hoffmann-Vold AM, Fretheim H, Halse AK, et al. Tracking impact of interstitial lung disease in systemic sclerosis in a complete nationwide cohort. Am J Respir Crit Care Med. 2019;200:1258–1266.
- Flaherty KR, Wells AU, Cottin V, et al. Nintedanib in progressive fibrosing interstitial lung diseases. N Engl J Med. 2019;381(18):1718-1727. doi:10.1056/NEJMoa1908681.
- Geerts S, Wuyts W, De Langhe E, et al. Connective tissue disease associated interstitial pneumonia: a challenge for both rheumatologists and pulmonologists. Sarcoidosis Vasc Diffuse Lung Dis. 2017;34(4):326–335.
- Wallace B, Vummidi D, Khanna D. Management of connective tissue diseases associated interstitial lung disease: a review of the published literature. Curr Opin Rheumatol. 2016;28(3):236–245.
