Resurse pentru echipa multidisciplinară
Echipele multidisciplinare pot juca un rol central în diagnosticul și managementul PID-BTC1,2

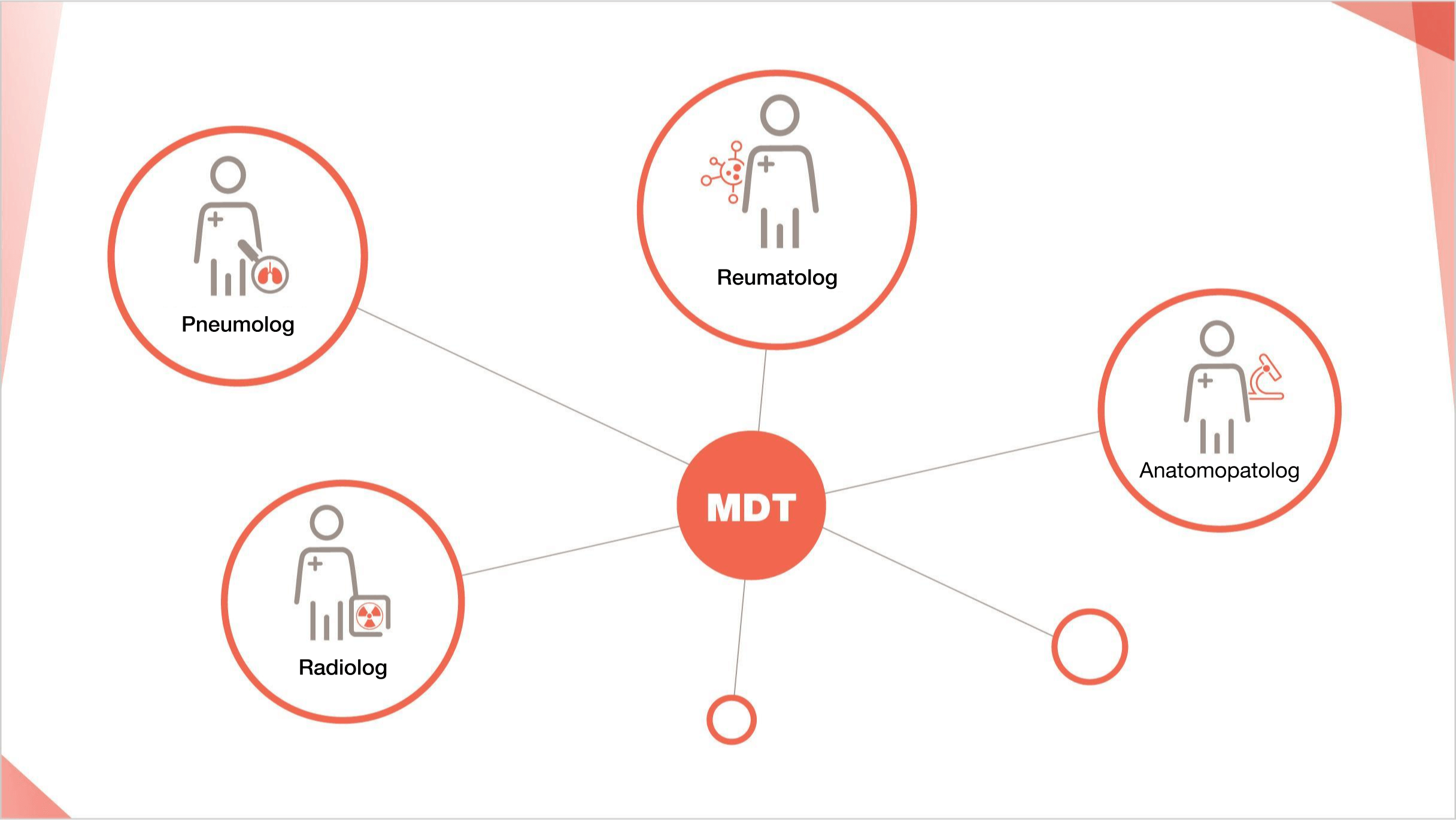
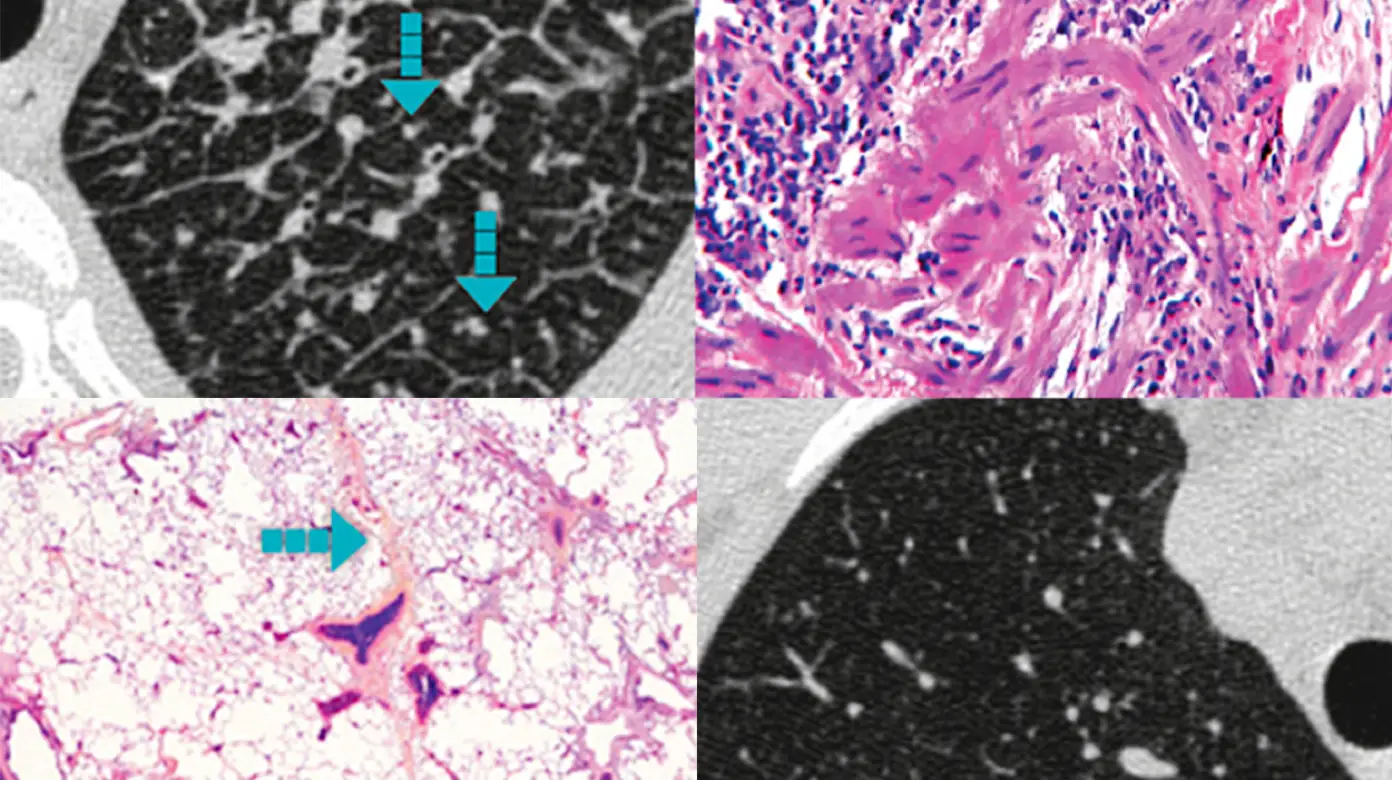
Colaborarea strânsă între reumatolog, pneumolog, radiolog și anatomopatolog este importantă în diagnosticul PID la pacienții cu BTC11 HRCT, și combinată cu discuțiile multidisciplinare, poate permite diagnosticarea confidentă PID în BTC.12-14 Diagnosticul multidisciplinar este asociat cu un nivel mai ridicat de încredere în diagnostic și un acord interobservator mai bun în comparație cu rolurile izolate14
O discuție multidisciplinară ar trebui inițiată la diagnosticarea PID la pacienții cu BTC, în timpul monitorizării acestora pentru a determina abordarea optimă pentru încetinirea progresiei bolii.1,15
În cazurile în care un MDT este dificil de convocat pentru un pacient cu PID, discuția multidisciplinară poate fi condusă virtual sau prin telefon pentru a permite fiecărui grup de specialitate să contribuie16
HRCT COMBINATĂ CU EVALUAREA MULTIDISCIPLINARĂ OFERĂ ÎNCREDERE MARE ÎN DIAGNOSTICUL PID LA PACIENȚII CU AR17-19
O abordare multidisciplinară, care include cel puțin un reumatolog, pneumolog și radiolog, îmbunătățește diagnosticul și gestionarea PID-AR17-20. Discuția multidisciplinară este recomandată pentru a confirma diagnosticul și a revizui severitatea PID-AR pe baza gradului de extensie a PID pe HRCT și DLCO21
Cadrul propus pentru evaluarea multidisciplinară a PID-AR17
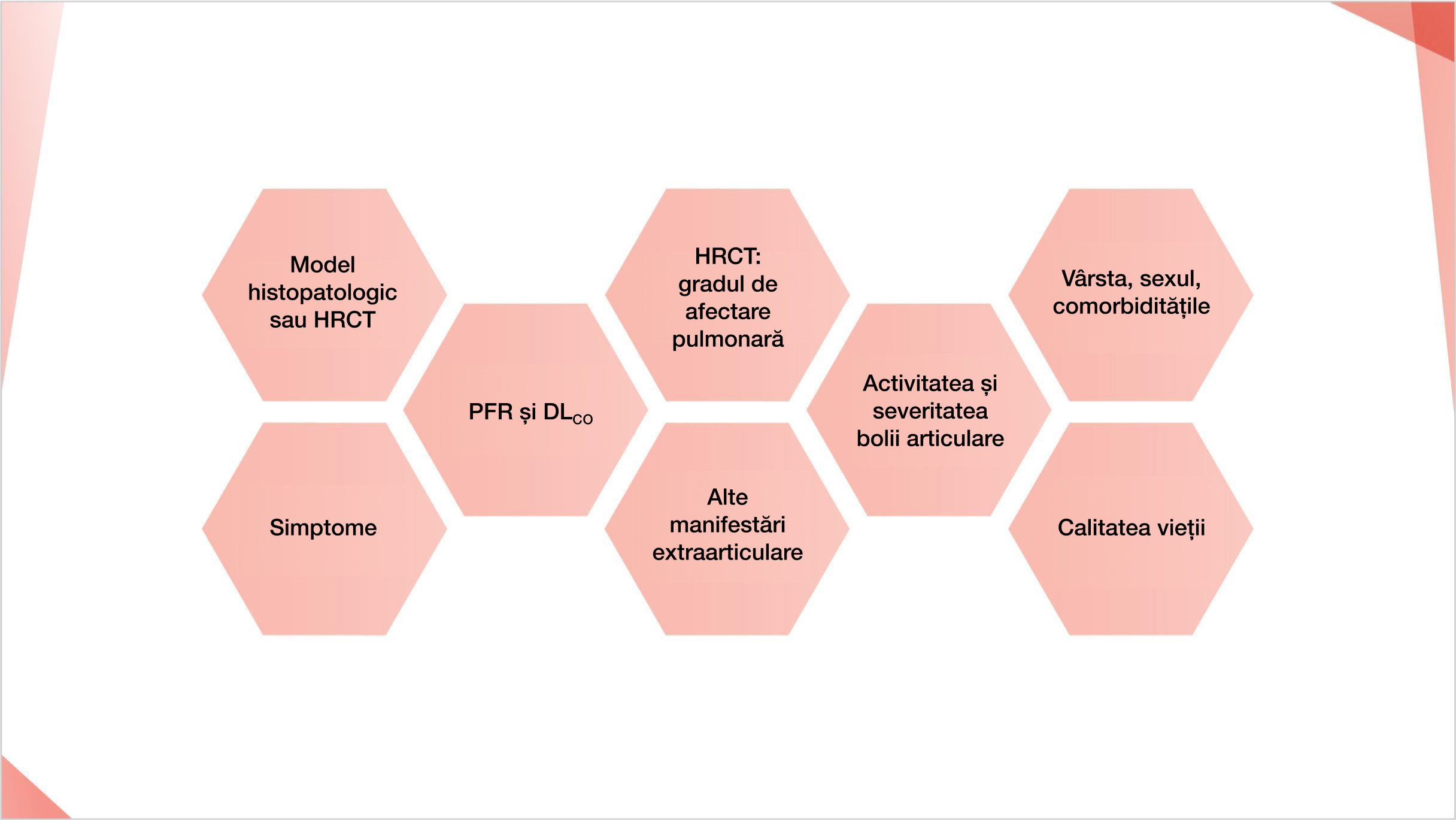
Adaptat după: Cassone G, et al. J Clin Med. 2020;9(4):1082.
RESURSE PENTRU ECHIPA MULTIDISCIPLINARĂ
RADIOLOGUL ARE UN ROL CENTRAL ÎN DIAGNOSTICUL PID-BTC ÎN COLABORAREA CU UN REUMATOLOG22
Istoricul clinic al pacienţilor cu BTC îl poate ajuta pe radiolog în:16
Contribuția la discuțiile în echipă multidisciplinară
Interpretarea caracteristicilor radiologice pe HRCT
Oferirea de informații valoroase pentru a face un diagnostic diferențial de PID
Iulia are PID-AR
Ce semne și simptome ridică suspiciunea de PID?
Ștefania are PID-ScS
Cum poți ajunge la un diagnostic de PID-ScS?
CUM PUTEȚI DA VESTEA UNUI DIAGNOSTIC DE PID PACIENȚILOR CU BTC?
A da o veste negativă pacienților este o sarcină de comunicare complexă. În seria noastră de filme documentare, profesorul Walter Baile, psihiatru și co-fondator al modelului SPIKES, ne prezintă prin abordarea sa practică cum să structurăm conversațiile dificile.
Modelul SPIKES presupune furnizarea de vești negative în practica clinică folosind șase elemente: Setare; Percepţie; Invitație/Informații; Cunoștinţe; empatie; Rezumat/Strategie26
CONVERSAȚII DIFICILE CU PACIENȚII DVS
Capitolul 1 – Provocarea de a comunica vești negative
Profesorul Walter Baile prezintă provocările pe care le implică comunicarea veștilor proaste și ceea ce putem învăța din experiența în oncologie.
Capitolul 2 – Modelul SPIKES în fibroza pulmonară
Comunicarea unui diagnostic cu compasiune poate face diferența. Vedeți de ce profesorul Walter Balle consideră că modelul SPIKES este relevant pentru fibroza pulmonară.
Capitolul 3 – Modelul SPIKES într-un scenariu real
Cuvintele contează. Profesorul Walter Balle descrie o experiență reală despre cum conversația plină de compasiune și sinceră a făcut diferența.
MODELUL SPIKES
Capitolul 1 – Modul SPIKES
O prezentare generală a fiecărui pas al modelului de comunicare SPIKES
Capitolul 2 – SPIKES: Setarea conversației
Configurarea conversației în mod corect pentru a vă ajuta pe dvs. și pacienții dvs. să se simtă relaxați.
Capitolul 3 – SPIKES: Percepția
Cum să determinați ce înțelege pacientul despre situația dată pentru a personaliza conversația.
Capitolul 4 – SPIKES: Invitația
Identificarea modului în care pacientul dvs. ar dori să primească veștile negative
Capitolul 5 – SPIKES: Cunoștințe
Aflați cum să oferiți faptele și informațiile pacientului dvs. într-un mod care funcționează pentru aceștia
Capitolul 6 – SPIKES: Emoții
Descoperiți cum să abordați emoțiile unui pacient cu un răspuns empatic.
Capitolul 7 – SPIKES: Strategie și rezumat
Modul în care elaborarea unui plan pentru viitor vă poate ajuta pacienții să se simtă informați și pregătiți.
Capitolul 8 – Ce vor pacienții de la medicii lor?
Profesorul Balle vă comunică cum să asigurați un parteneriat terapeutic deschis și onest cu pacienții dumneavoastră
Ce alte resurse vă pot ajuta să diagnosticați și să gestionați PID la pacienții dumneavoastră BTC?
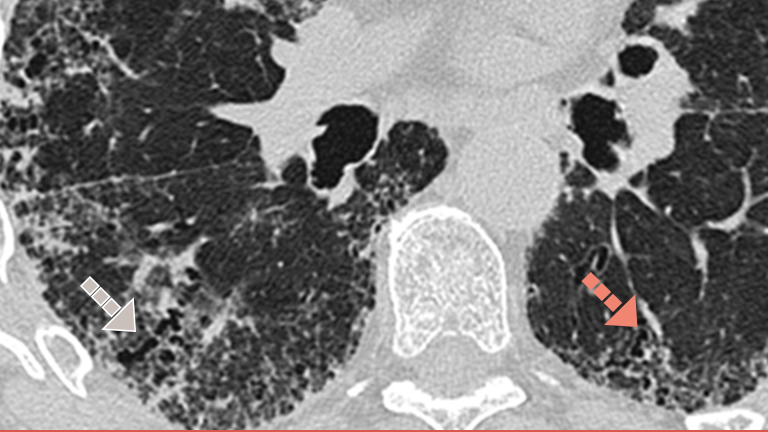
Investigarea PID-BTC fibrozante cu imagistica HRCT
Diagnosticul PID-BTC

Cazuri de pacienți PID-BTC pentru screening și diagnostic
Note
-
ACPA, anticorp anti-proteină citrulinată; ANA, anticorp antinuclear; CPK, creatin fosfokinaza; BTC, boli ale țesutului conjunctiv; PID-BTC, pneumopatie interstițială difuză asociată bolilor de țesut conjunctiv, DLCO, factorul de transfer gazos pentru monoxid de carbon, ds ADN, acid dezoxiribonucleic dublu catenar; eMDT, echipa multidisciplinară extinsă; HRCT, tomografie computerizata de înaltă rezoluție: PID, pneumopatie interstițială difuză; Pneumopatii interstițiale limfoide LIP MOAS, proteina 5 asociată diferențierii melanomului; MDT, echipa multidisciplinară; NSIP, pneumopatie interstițială nespecifică; OP, pneumopatie de organizare: polimiozita PM-Scl sclerodermie 70 kDa AR, artrita reumatoidă PID-AR, pneumopatie interstițială difuză asociată cu artrita reumatoidă; FR, factor reumatoid, Scl-70, sclerodermie 70 kDa; SPIKES, Setting-Perception - Invitație/ Informații - Cunoștințe - Empatie-Rezumat/Strategie; S5-A, antigenul sindromului Sjogren tip A; SS-B, antigenul de tip B al sindromului Sjögren; PID-ScS, pneumopatie interstițială difuză asociată sclerozei sistemice: ARNt, acid ribonucleic de transfer; UIP, pneumonie interstițială obișnuită.
- Wijsenbeek M, Cottin V. Spectrum of Fibrotic Lung Diseases. N Engl J Med. 2020;383:958–968.
- Kreuter M, Bendstrup E, Russell A, et al. Palliative care in interstitial lung disease: living well. Lancet Respir Med. 2017;5(12):968-980.
- Raghu G, Collard HR, Egan JJ, et al; on behalf of the ATS/ERS/JRS/ALAT Committee on Idiopathic Pulmonary Fibrosis. An official ATS/ERS/JRS/ALAT statement: idiopathic pulmonary fibrosis: evidence-based guidelines for diagnosis and management. Am J Respir Crit Care Med. 2011;183(6):788–824.
- Martinez FJ, Collard HR, Pardo A, et al. Idiopathic pulmonary fibrosis. Nat Rev. 2017;17:17074.
- Raghu G, Remy-Jardin M, Myers JL, et al; on behalf of the ATS/ERS/JRS/ALAT. Diagnosis of Idiopathic Pulmonary Fibrosis. An Official ATS/ERS/JRS/ALAT Clinical Practice Guideline. Am J Respir Crit Care Med. 2018;198(5):e44–e68.
- Molina-Molina M, Aburto M, Acosta O, et al. Importance of early diagnosis and treatment in idiopathic pulmonary fibrosis. Exp Rev Resp Med. 2018;12(7):537–539.
- Jo HE, Glaspole IN, Levin KC, et al. Clinical impact of the interstitial lung disease multidisciplinary service. Respirology. 2016;21(8):1438–1444.
- Cottin V, Hirani N, Hotchkin D, et al. Presentation, diagnosis and clinical course of the spectrum of progressive-fibrosing interstitial lung diseases. Eur Respir Rev. 2018;27(150):180076.
- Wong AW, Ryerson C, Guler S. Progression of fibrosing interstitial lung disease. Respir Res. 2020:29;21(1):32.
- De Sadeleer LJ, Meert C, Yserbyt J, et al. Diagnostic ability of a dynamic multidisciplinary discussion in interstitial lung diseases: A retrospective observational study of 938 cases. Chest. 2018;153(6):1416–1423.
- Dellaripa PF. Interstitial lung disease in the connective tissue diseases; a paradigm shift in diagnosis and treatment. Clin Immunol. 2018;186:71–73.
- Geerts S, Wuyts W, De Langhe E, et al. Connective tissue disease associated interstitial pneumonia: a challenge for both rheumatologists and pulmonologists. Sarcoidosis Vasc Diffuse Lung Dis. 2017;34(4):326–335.
- Wallace B, Vummidi D, Khanna D. Management of connective tissue diseases associated interstitial lung disease: a review of the published literature. Curr Opin Rheumatol. 2016;28(3):236–245.
- Walsh SLF. Multidisciplinary evaluation of interstitial lung diseases: current insights. Eur Respir Rev. 2017;26:170002.
- George PM, Spagnolo P, Kreuter M, et al. Progressive fibrosing interstitial lung disease: clinical uncertainties, consensus recommendations, and research priorities. Lancet Respir Med. 2020;8:925–954.
- Chung J, Goldin J. Interpretation of HRCT scans in the diagnosis of IPF: improving communication between pulmonologists and radiologists. Lung. 2018;196(5):561–567.
- Cassone G, Manfredi A, Vacchi C, et al. Treatment of rheumatoid arthritis-associated interstitial lung disease: lights and shadows. J Clin Med. 2020;9(4):1082. doi: 10.3390/jcm9041082.
- Iqbal K and Kelly C. Treatment of rheumatoid arthritis-associated interstitial lung disease: a perspective review. Ther Adv Musculoskelet Dis. 2015;7(6):247–267.
- Kawano-Dourado L, Doyle TJ, Bonfiglioli K, et al. Baseline characteristics and progression of a spectrum of interstitial lung abnormalities and disease in rheumatoid arthritis. Chest. 2020:S0012-3692(20)31412-4. doi: 10.1016/j.chest.2020.04.061.
- Castelino FV, Goldberg H, Dellaripa PF. The impact of rheumatological evaluation in the management of patients with interstitial lung disease. Rheumatology (Oxford). 2011;50:489–493.
- Lake F and Proudman S. Rheumatoid arthritis and lung disease: from mechanisms to a practical approach. Semin Respir Crit Care Med. 2014;35(2):222–238.
- De Lorenzis E, Bosello SL, Varone F, et al. Multidisciplinary Evaluation of Interstitial Lung Diseases: New Opportunities Linked to Rheumatologist Involvement. Diagnostics (Basel). 2020;10:664.
- Sverzellati N, Odone A, Silva M, et al. Structured reporting for fibrosing lung disease: a model shared by radiologist and pulmonologist. Radiol Med. 2018;123(4):245–253.
- Irion KL, Souza Jr AS, Marchiori E, da Silveira Dalla-Bona JP, Hochhegger B. Assessment of pulmonologists’ receptivity to a structured radiology report for interstitial lung disease. J Bras Pneumol. 2020;46(5):e20200164.
- Berkowitz EA, Bernheim A, Little BP. Introducing ILD-RADS: a pilot study of an interstitial lung disease standardized reporting template. J Am Coll Radiol. 2019;16(9 Pt A):1169–1172.
- Kaplan M. SPIKES: a framework for breaking bad news to patients with cancer. Clin J Oncol Nurs. 2010;14:514–516.