Managementul PID-ScS
Inițierea tratamentului la pacienții cu pneumopatie interstițială difuză asociată sclerozei sistemice (PID-ScS) ar trebui să vizeze prevenirea progresiei pentru a evita leziunile pulmonare ireversibile1–3


Ameliorați simptomele pacientului și îmbunătățiți calitatea vieții
Întârziați progresia PID

Prelungiți supraviețuirea
DE CE TREBUIE SĂ VIZĂM PREVENIREA PROGRESIEI LA PACIENȚII CU PID-ScS?
Practica actuală de tratare a pacienților cu PID-ScS odată ce a avut loc agravarea este sub-optimală.3 Acest lucru poate duce la pierderea oportunității de a trata pacienții a căror boală progresează, deoarece acești pacienți ar putea fi stabili în timpul urmăririi ulterioare. Pacienții cu PID-ScS cu dovezi de progresie continuă, bazată pe declinul funcției pulmonare sau deteriorarea radiografică, au nevoie de tratament independent de amploarea bolii.6
Algoritm de management clinic pentru PID-ScS2
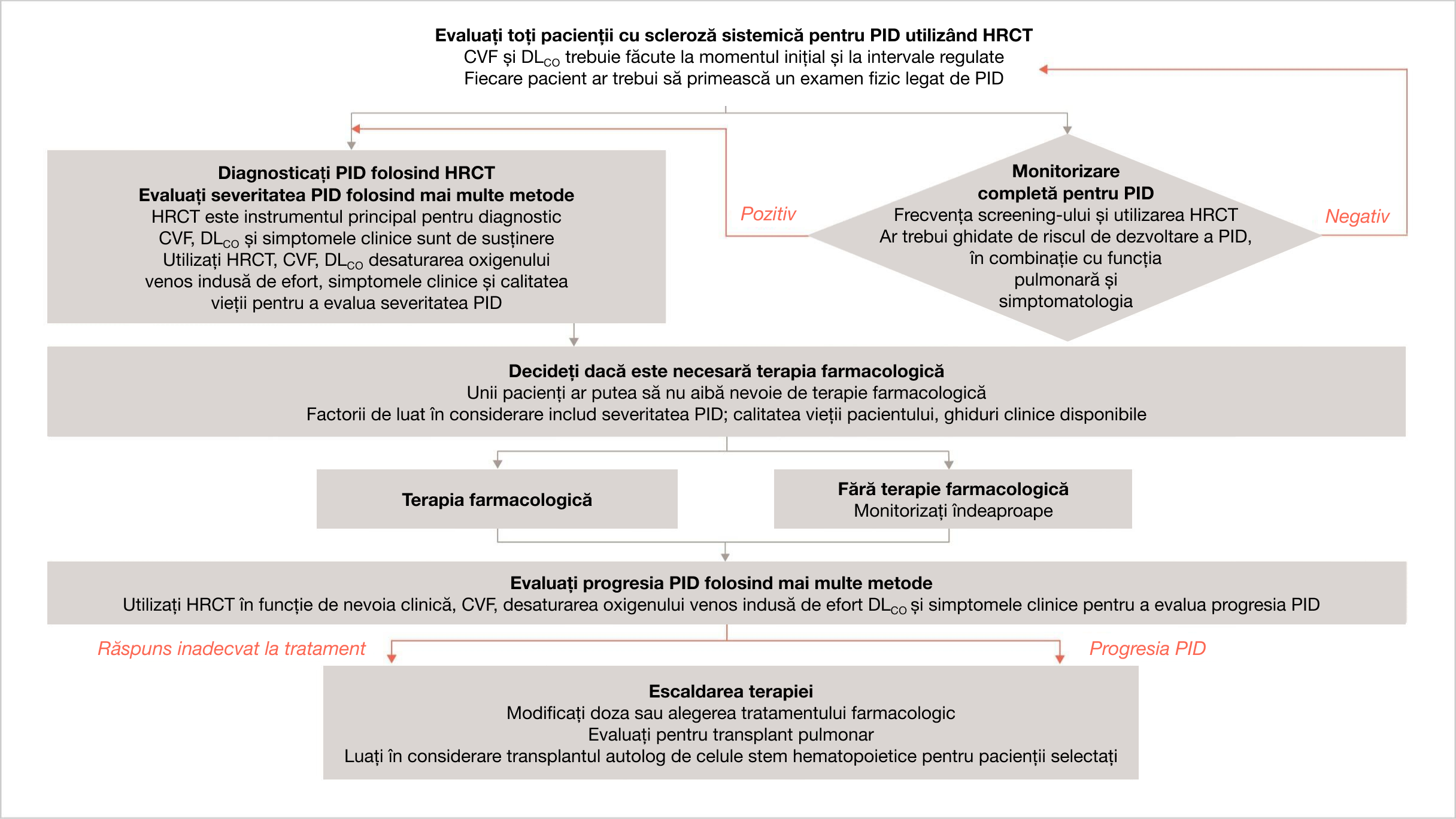
Acest algoritm oferă un scurt rezumat al declarațiilor de consens european bazate pe dovezi, inclusiv procesul suplimentar Delphi, din opinia experților a comitetului de coordonare pentru identificarea și gestionarea PID-ScS, pentru utilizare în practica clinică.
Adaptat după Hoffmann-Vold AM, et al. Lancet Rheum. 2020;2:e71-e83.
O ABORDARE MULTIDISCIPLINARĂ DE ECHIPĂ OPTIMIZEAZĂ EVALUAREA ȘI ÎNGRIJIREA PACIENȚILOR CU PID-SCS2,7,8
Datorită implicării mai multor organe în ScS și naturii complexe a PID-ScS, angajamentul multidisciplinar este cheia pentru a oferi îngrijiri optime pacienților.8
Exemplu de echipă multidisciplinară pentru managementul PID-ScS
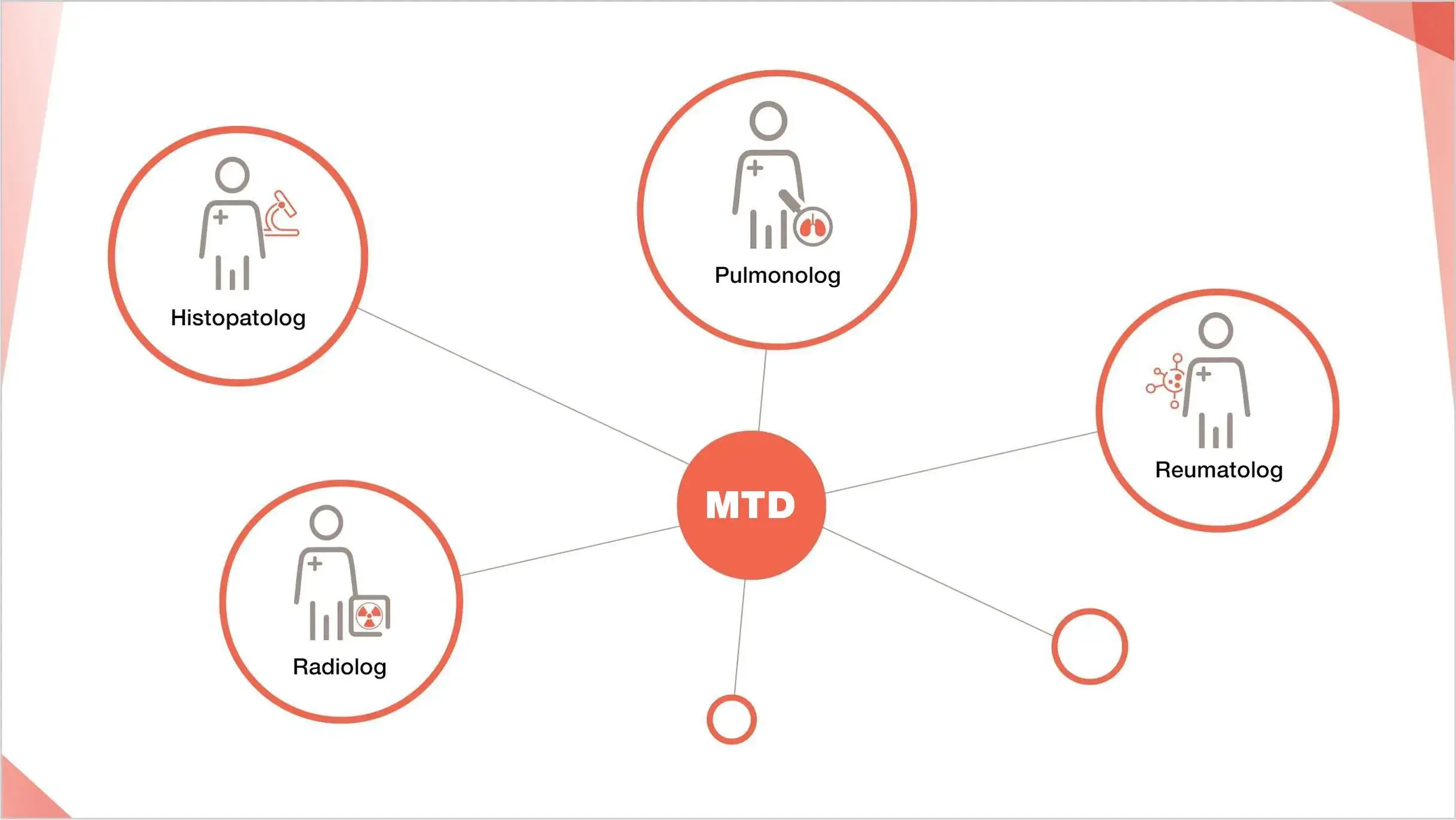
Recomandările managementului clinic optim al pacienților cu PID-ScS poate fi realizată prin încorporarea colaborării între reumatologi, pneumologi și interniști2
De ce alte considerente de management ar trebui să țineți cont?

Monitorizarea continuă în PID-ScS

Oferirea de îngrijiri paliative/ de susținere

Echipa multidisciplinară
Note
-
PID-BTC, pneumopatie interstițială difuză asociată cu boli ale țesutului conjunctiv; DLCO, factorul de transfer gazos pentru monoxid de carbon; CVF, capacitate vitală forțată; HRCT, tomografie computerizată de înaltă rezoluție; PID, pneumopatie interstițială difuză; ScS, scleroză sistemică; PID-ScS, pneumopatie interstițială difuză asociată sclerozei sistemice.
- Hoffmann-Vold AM, Allanore Y, Alves M, et al. Progressive interstitial lung disease in patients with systemic sclerosis-associated interstitial lung disease in the EUSTAR database. Ann Rheum Dis. 2020;217455.
- Hoffmann-Vold AM, Maher TM, Philpot EE, et al. The identification and management of interstitial lung disease in systemic sclerosis: evidence-based European consensus statements. Lancet Rheum. 2020;2:e71–e83.
- Distler O, Volkmann ER, Hoffmann-Vold AM, et al. Current and future perspectives on management of systemic sclerosis-associated interstitial lung disease. Expert Rev Clin Immunol. 2019;15:1009–1017.
- Guler, S.A., Winstone, T.A., Murphy, D., et al. Does systemic sclerosis–associated interstitial lung disease burn out? Specific phenotypes of disease progression. Annals ATS. 2018;15;1427–1433.
- Hoffmann-Vold AM, Fretheim H, Halse AK, et al. Tracking impact of interstitial lung disease in systemic sclerosis in a complete nationwide cohort. Am J Respir Crit Care Med. 2019;200;1258–1266.
- Cappelli S, Bellando Randone S, Camiciottoli G, et al. Interstitial lung disease in systemic sclerosis: where do we stand? Eur Respir Rev. 2015;24;411–419.
- Roofeh D, Jaafar S, Vummidi D, et al. Management of systemic sclerosis-associated interstitial lung disease. Curr Opin Rheumatol. 2019;31;241–249.
- Fischer A, Patel NM, Volkmann ER. Interstitial lung disease in systemic sclerosis: focus on early detection and intervention. OARRR. 2019;11;283–307.
- Distler O, Assassi S, Cottin V, et al. Predictors of progression in systemic sclerosis patients with interstitial lung disease. Eur Respir J. 2020;55;1902026.
- Ryerson CJ, Cayou C, Topp F, et al. Pulmonary rehabilitation improves long-term outcomes in interstitial lung disease: a prospective cohort study. Respir Med. 2014;108(1):203-210.
- Kreuter M, Bendstrup E, Russell A, et al. Palliative care in interstitial lung disease: living well. Lancet Respir Med. 2017;5(12):968-980.
- Maher TM, Wuyts W. Management of Fibrosing Interstitial Lung Diseases. Adv Ther. 2019;doi:10.1007/s12325-019-00992-9. [Epub ahead of print].
- Sgalla G, Cerri S, Ferrari R, et al. Mindfulness-based stress reduction in patients with interstitial lung diseases: a pilot, single-centre observational study on safety and efficacy. BMJ Open Respir Res. 2015;2(1):e000065.
- Wijsenbeek M, Cottin V. Spectrum of Fibrotic Lung Diseases. N Engl J Med. 2020;383:958–968.
